
ÌâÄ¿Áбí(°üÀ¨´ð°¸ºÍ½âÎö)
8£®ÏÂÁÐ˵·¨ÖÐÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡)
A£®ÈκÎÔ×Ó¼°ÆäÀë×Ó£¬¶¼ÊǺËÍâµç×Ó²ãÊýµÈÓÚ¸ÃÔªËØÔÚÖÜÆÚ±íÖеÄÖÜÆÚÊý
B£®ÔÚÔªËØÖÜÆÚ±íÖУ¬´Ó¢óB×åµ½¢òA×åµÄ10¸ö×ÝÁÐÖУ¬ËùÓеÄÔªËض¼ÊǽðÊôÔªËØ
C£®ËùÓÐÏ¡ÓÐÆøÌåÔªËصÄÔ×ÓµÄ×îÍâ²ãµç×ÓÊý¶¼ÊÇ8
D£®·²ÊÇͬÖÖÔªËصÄͬλËØ£¬Æä¸÷ÏîÎïÀíÐÔÖÊ¡¢»¯Ñ§ÐÔÖʶ¼Ïàͬ
´ð°¸£ºB
7£®ÒÑÖªX¡¢Y¡¢Z 3ÖÖÖ÷×åÔªËØÔÚÔªËØÖÜÆÚ±íÖеÄÏà¶ÔλÖÃÈçͼËùʾ£¬ÉèXµÄÔ×ÓÐòÊýΪa£¬ÔòÏÂÁÐ˵·¨Öв»ÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡)
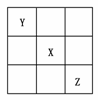
A£®YÓëZµÄÔ×ÓÐòÊýÖ®ºÍ¿ÉÄÜΪ2a
B£®YµÄÔ×ÓÐòÊý¿ÉÄÜΪa£19
C£®ZµÄÔ×ÓÐòÊý¿ÉÄÜΪa+33
D£®X¡¢Y¡¢ZÒ»¶¨¶¼ÊǶÌÖÜÆÚÔªËØ
´ð°¸£ºD
6£®(2008¡¤¹ã¶«¸ß¿¼)ÏÂÁÐÓйØÔ×ӽṹºÍÔªËØÖÜÆÚÂɵıíÊöÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡)
¢ÙÔ×ÓÐòÊýΪ15µÄÔªËصÄ×î¸ß»¯ºÏ¼ÛΪ+3
¢Ú¢÷A×åÔªËØÊÇͬÖÜÆÚÖзǽðÊôÐÔ×îÇ¿µÄÔªËØ
¢ÛµÚ¶þÖÜÆÚ¢ôA×åÔªËصÄÔ×Ӻ˵çºÉÊýºÍÖÐ×ÓÊýÒ»¶¨Îª6
¢ÜÔ×ÓÐòÊýΪ12µÄÔªËØλÓÚÔªËØÖÜÆÚ±íµÄµÚÈýÖÜÆÚ¢òA×å
A£®¢Ù¢Ú¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®¢Ù¢Û
C£®¢Ú¢Ü¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®¢Û¢Ü
´ð°¸£ºC
5£®ÏÂÁйØÓÚÔªËØÖÜÆÚ±íµÄÐðÊö£¬²»ÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡)
A£®¹²ÓÐ7¸öÖÜÆÚ£¬16¸ö×å
B£®Ðγɻ¯ºÏÎïÖÖÀà×î¶àµÄÔªËØÔÚµÚ2ÖÜÆÚ
C£®¢òA×åµÄÓÒ±ßÊÇ¢óB×壬¢òA×åµÄ×ó±ßÊÇ¢òB×å
D£®Ä³Ö÷×åÔªËØ×î¸ß¼ÛÑõ»¯Îï¶ÔÓ¦µÄË®»¯ÎïµÄ»¯Ñ§Ê½ÎªHnROm£¬ÆäÆø̬Ç⻯ÎïµÄ»¯Ñ§Ê½Ò»¶¨ÎªH2m£nR»òRH2m£n
½âÎö£ºÔÚHnROmÖÐRÔªËصĻ¯ºÏ¼ÛΪ+(2m£n)£¬ÔòÆäÆø̬Ç⻯ÎïÖÐRÔªËصĻ¯ºÏ¼ÛӦΪ£(8£2m+n)£¬Òò´Ë£¬ÆäÆø̬Ç⻯ÎïµÄ»¯Ñ§Ê½Ó¦ÎªH8£2m+nR»òRH8£2m+n¡£
´ð°¸£ºD
4£®(2009¡¤ÉϺ£Ê¦´ó¸½ÖÐÄ£Äâ)¾Ý¹úÍâ×ÊÁϱ¨µÀ£¬ÔÚ¶À¾Óʯ(Ò»ÖÖ¹²Éú¿ó£¬»¯Ñ§³É·ÖΪCe¡¢La¡¢NdµÈµÄÁ×ËáÑÎ)ÖУ¬²éÃ÷ÓÐÉÐδÃüÃûµÄ116¡¢124¡¢126ºÅÔªËØ¡£ÅжÏÆäÖÐ116ºÅӦλÓÚÖÜÆÚ±íÖеġ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡)
A£®µÚÁùÖÜÆÚ¢ôA×å¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®µÚÆßÖÜÆÚ¢öA×å
C£®µÚÆßÖÜÆÚ¢ø×å¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®µÚ°ËÖÜÆÚ¢öA×å
´ð°¸£ºB
3£®Ëæ×űËØÔ×Ӱ뾶µÄÔö´ó£¬ÏÂÁеݱä¹æÂÉÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡)
A£®µ¥ÖʵÄÈ۷еãÖð½¥½µµÍ
B£®Â±ËØÀë×ӵĻ¹ÔÐÔÖð½¥ÔöÇ¿
C£®Æø̬Ç⻯ÎïÎȶ¨ÐÔÖð½¥ÔöÇ¿
D£®µ¥ÖÊÑõ»¯ÐÔÖð½¥ÔöÇ¿
´ð°¸£ºB
2£®(2009¡¤ÎߺþÒ»ÖиßÈýһģ)È«¹ú¿Æѧ¼¼ÊõÃû´ÊÉó¶¨Î¯Ô±2007Äê3ÔÂ21ÈÕ¹«²¼£º111ºÅÔªËØ(·ûºÅΪRg)µÄÖÐÎÄÃû³ÆΪ¡°îÄÂØ¡±(¶ÁÒôΪÂ×)¡£ÏÂÁÐ˵·¨ÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡)
A£®111ºÅÔªËØÊǵÚ6ÖÜÆÚ¢ñA×åµÄ½ðÊôÔªËØ
B£®111ºÅÔªËØÊôÓÚ¹ý¶ÉÔªËØ
C£®111ºÅÔªËØΪ·Ç½ðÊôÔªËØ
D£®111ºÅÔªËØÖÊÁ¿ÊýΪ111
´ð°¸£ºB
1£®¼òµ¥Ô×ÓµÄÔ×ӽṹ¿ÉÓÃÏÂͼÐÎÏóµØ±íʾ
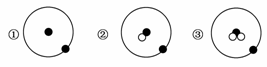
ÆäÖСñ±íʾÖÊ×Ó»òµç×Ó£¬¡ð±íʾÖÐ×Ó£¬ÔòÏÂÁÐÓйآ٢ڢ۵ÄÐðÊöÕýÈ·µÄ×éºÏÊÇ
(¡¡)
a£®¢Ù¢Ú¢Û»¥ÎªÍ¬Î»ËØ
b£®¢Ù¢Ú¢Û»¥ÎªÍ¬ËØÒìÐÎÌå
c£®¢Ù¢Ú¢ÛÊÇÈýÖÖ»¯Ñ§ÐÔÖʲ»Í¬µÄÁ£×Ó
d£®¢Ù¢Ú¢Û¾ßÓÐÏàͬµÄÖÊÁ¿Êý
e£®¢Ù¢Ú¢Û¾ßÓÐÏàͬµÄÖÊÁ¿
f£®¢Ù¢Ú¢ÛÊÇÈýÖÖ²»Í¬µÄÔ×Ó
A£®a¡¢f¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®b¡¢c
C£®d¡¢e¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®e¡¢f
´ð°¸£ºA
20£®(2009¡¤¸£½¨)¶ÌÖÜÆÚÔªËØQ¡¢R¡¢T¡¢WÔÚÔªËØÖÜÆÚ±íÖеÄλÖÃÈçͼËùʾ£¬ÆäÖÐTËù´¦µÄÖÜÆÚÐòÊýÓëÖ÷×åÐòÊýÏàµÈ£¬Çë»Ø´ðÏÂÁÐÎÊÌ⣺
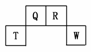
(1)TµÄÔ×ӽṹʾÒâͼΪ__________________________________________________¡£
(2)ÔªËصķǽðÊôÐÔ(Ô×ӵĵõç×ÓÄÜÁ¦)Ϊ£ºQ________(Ìî¡°Ç¿ÓÚ¡±»ò¡°ÈõÓÚ¡±)W¡£
(3)WµÄµ¥ÖÊÓëÆä×î¸ß¼ÛÑõ»¯ÎïµÄË®»¯ÎïŨÈÜÒº¹²ÈÈÄÜ·¢Éú·´Ó¦£¬Éú³ÉÁ½ÖÖÎïÖÊ£¬ÆäÖÐÒ»ÖÖÊÇÆøÌ壬·´Ó¦µÄ»¯Ñ§·½³ÌʽΪ____________________________________________¡£
(4)Ô×ÓÐòÊý±ÈR¶à1µÄÔªËصÄÒ»ÖÖÇ⻯ÎÄÜ·Ö½âΪËüµÄÁíÒ»ÖÖÇ⻯Î´Ë·Ö½â·´Ó¦µÄ»¯Ñ§·½³ÌʽÊÇ
________________________________________________________________________¡£
(5)RÓжàÖÖÑõ»¯ÎÆäÖм׵ÄÏà¶Ô·Ö×ÓÖÊÁ¿×îС¡£ÔÚÒ»¶¨Ìõ¼þÏ£¬2LµÄ¼×ÆøÌåÓë0.5 LµÄÑõÆøÏà»ìºÏ£¬Èô¸Ã»ìºÏÆøÌå±»×ãÁ¿µÄNaOHÈÜÒºÍêÈ«ÎüÊÕºóûÓÐÆøÌå²ÐÁô£¬ËùÉú³ÉµÄRµÄº¬ÑõËáÑεĻ¯Ñ§Ê½ÊÇ___________________________________________________¡£
(6)ÔÚ298 KÏ£¬Q¡¢TµÄµ¥Öʸ÷1 molÍêȫȼÉÕ£¬·Ö±ð·Å³öÈÈÁ¿a kJºÍb kJ¡£ÓÖÖªÒ»¶¨Ìõ¼þÏ£¬TµÄµ¥ÖÊÄܽ«Q´ÓËüµÄ×î¸ß¼ÛÑõ»¯ÎïÖÐÖû»³öÀ´£¬Èô´ËÖû»·´Ó¦Éú³É3 mol QµÄµ¥ÖÊ£¬Ôò¸Ã·´Ó¦ÔÚ298 KϵĦ¤H£½________(×¢£ºÌâÖÐËùÉèµ¥ÖʾùΪ×îÎȶ¨µ¥ÖÊ)
½âÎö£ºÓÉÐÅÏ¢¿ÉÖª£¬TΪµÚ3ÖÜÆÚ¢óA×åÔªËØ£¬¼´ÎªAl£º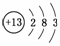 £¬Q£¬R£¬W·Ö±ðΪC¡¢N¡¢S£¬Ôò(1)¡¢(2)¡¢(3)¡¢(4)Ò×½â´ð£»(5)ÖÐNµÄÑõ»¯ÎïÖÐÏà¶Ô·Ö×ÓÖÊÁ¿×îСµÄΪNO£¬(6)C(s)+O2(g)===CO2(g)£»¦¤H£½£a kJ/mol£¬¡¡¢Ù
£¬Q£¬R£¬W·Ö±ðΪC¡¢N¡¢S£¬Ôò(1)¡¢(2)¡¢(3)¡¢(4)Ò×½â´ð£»(5)ÖÐNµÄÑõ»¯ÎïÖÐÏà¶Ô·Ö×ÓÖÊÁ¿×îСµÄΪNO£¬(6)C(s)+O2(g)===CO2(g)£»¦¤H£½£a kJ/mol£¬¡¡¢Ù
Al(s)+O2(g)===Al2O3(s)£»¦¤H£½£b kJ/mol£¬¡¡¢Ú
Ôò·´Ó¦4Al(s)+3CO2(g)===3C(s)+2Al2O3(s)Ϊ¦¤H£½¢Ú¡Á4£¢Ù¡Á3£½(3a£4b)kJ/mol¡£
´ð°¸£º(1)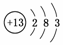 ¡¡(2)ÈõÓÚ
¡¡(2)ÈõÓÚ
(3)S+2H2SO4(Ũ)3SO2¡ü+2H2O
(4)2H2O22H2O+O2¡ü
(5)NaNO2
(6)(3a£4b) kJ¡¤mol£1
19£®(2009¡¤Ìì½ò)ϱíΪԪËØÖÜÆÚ±íµÄÒ»²¿·Ö£¬Çë²ÎÕÕÔªËØ¢Ù-¢àÔÚ±íÖеÄλÖã¬Óû¯Ñ§ÓÃÓï»Ø´ðÏÂÁÐÎÊÌ⣺
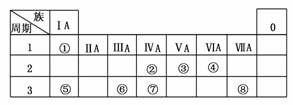
(1)¢Ü¢Ý¢ÞµÄÔ×Ӱ뾶ÓÉ´óµ½Ð¡µÄ˳ÐòÊÇ____________________________________¡£
(2)¢Ú¢Û¢ßµÄ×î¸ß¼Ûº¬ÑõËáµÄËáÐÔÓÉÇ¿µ½ÈõµÄ˳ÐòÊÇ
________________________________________________________________________¡£
(3)¢Ù¢Ü¢Ý¢àÖеÄijЩԪËØ¿ÉÐγɼȺ¬Àë×Ó¼üÓÖº¬¼«ÐÔ¹²¼Û¼üµÄ»¯ºÏÎд³öÆäÖÐÒ»ÖÖ»¯ºÏÎïµÄµç×Óʽ£º
________________________________________________________________________¡£
(4)ÓɱíÖÐÁ½ÖÖÔªËصÄÔ×Ó°´1?1×é³ÉµÄ³£¼ûҺ̬»¯ºÏÎïµÄÏ¡ÈÜÒºÒ×±»´ß»¯·Ö½â£¬¿ÉʹÓõĴ߻¯¼ÁΪ(ÌîÐòºÅ)________¡£
a£®MnO2¡¡b£®FeCl3¡¡c£®Na2SO3¡¡d£®KMnO4
(5)ÓɱíÖÐÔªËØÐγɵij£¼ûÎïÖÊX¡¢Y¡¢Z¡¢M¡¢N¿É·¢ÉúÒÔÏ·´Ó¦£º

XÈÜÒºÓëYÈÜÒº·´Ó¦µÄÀë×Ó·½³ÌʽΪ________________________________________£¬
N¡ú¢ÞµÄµ¥ÖʵĻ¯Ñ§·½³ÌʽΪ_______________________________________________£¬
³£ÎÂÏ£¬ÎªÊ¹0.1 mol/L MÈÜÒºÖÐÓÉMµçÀëµÄÒõ¡¢ÑôÀë×ÓŨ¶ÈÏàµÈ£¬Ó¦ÏòÈÜÒºÖмÓÈëÒ»¶¨Á¿µÄYÈÜÒºÖÁ
________________________________________________________________________¡£
½âÎö£º¾ÝÔªËصÄλÖÿÉÖª£¬¢Ù-¢àÔªËØÒÀ´ÎΪH¡¢C¡¢N¡¢O¡¢Na¡¢Al¡¢Si¡¢Cl£¬ÔÙ¶ÔºÅÈë×ù£¬ÆäÖÐ(5)ÓÉ¿òͼ¿ÉÈ·¶¨NΪAl2O3£¬ZΪAl(OH)3¡£MӦΪNH4Cl£¬ÔòX¡¢YΪAlCl3¡¢NH3¡¤H2O£¬ÎªÊ¹NH4ClÖÐÓÉNH4ClµçÀë³öµÄc(NH)£½c(Cl£)¿É¼ÓÈëNH3¡¤H2O(Y)ÖÁÈÜÒºpHµÈÓÚ7¡£
´ð°¸£º(1)Na>Al>O¡¡(2)HNO3>H2CO3>H2SiO3
(3)Na+[¡Ã¡¤¡¤¡¤¡¤¡¬H]£(»òNa+[¡Ã¡¤¡¤¡¤¡¤¡Ã¡¤¡¤¡¤¡¤¡Ã]£)
(4)a¡¢b¡¡(5)Al3++3NH3¡¤H2O===Al(OH)3¡ý+3NH
2Al2O3(ÈÛÈÚ)µç½â±ù¾§Ê¯4Al+3O2¡ü¡¡ÈÜÒºµÄpHµÈÓÚ7
¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com