
题目列表(包括答案和解析)
13.
在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用图中的实验装置进行实验,证明过氧化钠可作供氧剂。
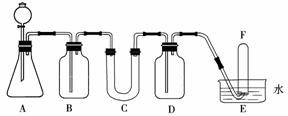
(1)A是制取CO2的装置。写出A中发生反应的化学方程式: 。
(2)填写表中空格:
|
仪器 |
加入试剂 |
加入该试剂的目的 |
|
B |
饱和NaHCO3溶液 |
|
|
C |
|
|
|
D |
|
|
(3)写出过氧化钠与二氧化碳反应的化学方程式: 。
(4)试管F中收集满气体后,下一步实验操作是 。
12. 某干燥粉末可能由Na2O、Na2O2、Na2CO3、NaHCO3、NaCl中的一种或几种组成。将该粉末与足量的盐酸反应有气体X逸出,X通过足量的NaOH溶液后体积缩小(同温、同压下测定)。若将原混合粉末在空气中用酒精灯加热,也有气体放出,且剩余固体的质量大于原混合粉末的质量。下列判断正确的是()
A. 粉末中一定只含有Na2O、NaHCO3
B. 粉末中一定不含有Na2CO3和NaCl
C. 粉末中一定不含有Na2O和NaCl
D. 无法肯定粉末里是否含有Na2CO3和NaCl
11. (2007年高考全国卷Ⅱ)在一定条件下,将钠与氧气反应的生成物1.5 g溶于水,所得溶液恰好能被80 mL浓度为0.50 mol/L的HCl溶液中和,则该生成物的成分是()
A. Na2OB. Na2O2
C. Na2O和Na2O2D. Na2O2和NaO2
10. 将1 mol Na2O2和1 mol NH4HCO3的固体混合后置于密闭容器中,加热至300 ℃,待完全反应后放出气体,残余的固体物质是( )
A. 1 mol Na2CO3和1 mol NaOH
B. 1 mol Na2CO3
C. 0.5 mol Na2CO3和0.5 mol NaOH
D. 1 mol NaOH
9. (2008年高考北京卷)1 mol过氧化钠与2 mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是( )
A. Na2CO3
B. Na2O2 Na2CO3
C. NaOH Na2CO3
D. Na2O3 NaOH Na2CO3
8. 200 ℃时,11.6 g由CO2和H2O组成的混合气体与足量Na2O2充分反应后,固体质量增加3.6 g,则原混合气体的平均相对分子质量为( )
A. 5.8B. 11.6C. 23.2D. 46.4
7. 等物质的量的N2、O2、CO2混合气体通过Na2O2后,体积变为原体积的89(同温同压),这时混合气体中N2、O2、CO2物质的量之比为( )
A. 3∶4∶1
B. 3∶3∶2
C. 6∶7∶3
D. 6∶9∶0
6. 2.1 g平均相对分子质量为7.2的CO与H2组成的混合气体与足量的O2充分燃烧后,立即通入足量的Na2O2固体中,固体的质量增加( )
A. 2.1 gB. 3.6 g
C. 7.2 gD. 无法确定
5. 下列有水参加的反应中,属于氧化还原反应,但水既不是氧化剂,又不是还原剂的是( )
A. 金属钠和水反应
B. 氧化钠和水反应
C. 过氧化钠和水反应
D. CO2+H2O+Na2CO3=2NaHCO3
4. 3.72 g过氧化钠、氧化钠和钠的混合物,与足量的水反应在标准状况下生成V mL混合气体,该混合气体在一定条件下恰好完全反应。则混合物中Na、Na2O、Na2O2的质量之比为( )
A. 23∶1∶39B. 1∶1∶1
C. 1∶2∶1D. 1∶2∶4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com