
题目列表(包括答案和解析)
10.由-OH、-CH3、-C6H5、-CHO、-COOH等五种基团构成的物质中,其中能与NaOH溶液反应的有机物有
A.4种 B.5种 C.6种 D.7种
9.将pH=1的醋酸溶液加水稀释至pH=3后,下列说法正确的是
A.电离平衡向右移动,c(CH3COO-)增大
B.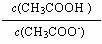 的比值不变
的比值不变
C.溶液中离子的总物质的量不变
D.溶液中的c (OH- )增大
8.下列各组离子在指定条件下,一定能大量共存的是
A.能使红色石蕊试纸显蓝色的溶液:K+、Na+、SO42-、C2O42-
B.能使碘化钾淀粉试纸变蓝的溶液:Na+、NH4+、S2-、Br-
C.水电离出的c(H+)=10-12mol/L的溶液:Ba2+、Na+、NO3-、HCO3-
D.加入铝条有氢气放出的溶液:Na+、NH4+、Cl-、NO3-
7.有t℃的a g KCl不饱和溶液,其质量分数为w1,采取措施后使其变为b g饱和溶液,其溶质质量分数为w2,下列说法正确的是
A.a一定小于或等于b B.aw1一定等于b w2 C.t℃时KCl溶解度一定大于100w1 D.w1一定大于w2
6.“节约资源、保护环境”是科学发展观的基本要求。下述操作不是从科学发展观角度考虑的是
A.工业合成氨中分离产物得到的氢气和氮气再循环使用
B.用稀硝酸代替浓硝酸溶解、回收做完银镜实验后试管内壁的银
C.接触法制硫酸的设备中安装“热交换器”,利用余热预热冷原料气
D.实验室短时间保存硫酸亚铁溶液时,向试剂瓶中添加少量铁粉和稀硫酸
27.(10分)A、B、C、D为前四周期元素。A元素的原子价电子排布为ns2np2,B元素的最外层电子数是其电子层数的3倍,C元素原子的M能层的p能级有3个未成对电子,D元素原子核外的M能层中只有2对成对电子。
(1)当n=2时,AB2属于 分子(填“极性”或“非极性”),分子中有 个σ键,
个π键。A6H6分子中A原子的杂化轨道类型是 杂化。
(2)当n =3时, A与B形成的晶体属于 晶体。
(3)若A元素的原子价电子排布为3s23p2,A、C、D三种原子的电负性由大到小的顺序是
(用元素符号表示),A、C、D三种元素的第一电离能由大到小的顺序是 (用元素符号表示)。
(4)已知某红紫色络合物的组成为CoCl3·5NH3·H2O。该络合物中的中心离子钴离子在基态时核外电子排布式为 ,作为配位体之一的NH3分子的空间构型为 。
26.(10分)已知:(1)在NaOH的水溶液中有以下转化:
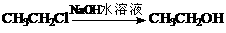
(2)一个碳原子上连有两个羟基或碳碳双键上连有羟基时,易发生下列转化:
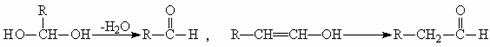
请根据下图作答:
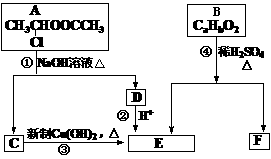
(1) E中含有的官能团的名称是______________________。
(2) 反应⑧的化学方程式__________________________________________________。
(3) 已知B的相对分子质量为162,其完全燃烧的产物中n(CO2):n(H2O)=2:1,则B
的化学式为__________________。
(4)若 F具有如下特点:
Ⅰ、①能跟FeCl3溶液发生显色反应;②能发生加聚反应:③苯环上的一氯代物只有两种。则F在一定条件下发生加聚反应的化学方程式为_______________________________________;
Ⅱ、①为苯的一取代物;②能发生银镜反应。则F的结构简式为 。
25.(9分)丙烯是石油化工的重要原料,一定条件下可发生下列转化:
已知: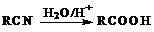 ;
R-Br+NaOH→R-OH+NaBr
;
R-Br+NaOH→R-OH+NaBr
(1)A的结构简式为:____________;
(2)反应④的类型为:_________________反应;
(3)D与足量乙醇反应生成E的化学方程式为:_______________________________。
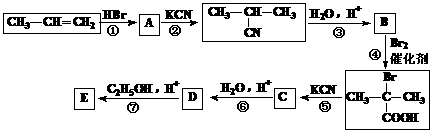
(4)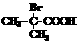 与足量NaOH溶液反应的化学方程式为____________________________。
与足量NaOH溶液反应的化学方程式为____________________________。
(5)B的同分异构体有多种.写出其中既能发生银镜反应,又能发生酯化反应的2种同分异
构体的结构简式:__________________、___________________。
24.(10分)水体中二价汞离子可以与多种阴离子结合成不同的存在形态。水溶液中二价汞主要存在形态与Cl-、OH-的浓度关系如右图所示 [注:粒子浓度很小时常用负对数表示,如
pH=-lgc(H+),pCl=-lgc(Cl-)]。
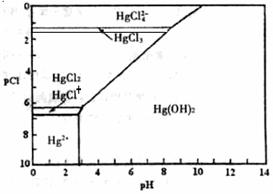
(1)正常海水(Cl-的浓度大于0.1mol/L)中汞元素的主要存在形态是 。少量Hg(NO3)2溶于0.001mol/L的盐酸后得到无色透明溶液,其中汞元素的主要存在形态是 。
(2)Hg(NO3)2固体易溶于水,但溶于水时常常会出现浑浊,其原因是 (用离子方程式表示),为了防止出现浑浊,可采取的措施是 。
(3)处理含汞废水的方法很多。下面是常用的两种方法,汞的回收率很高。
① 置换法:用废铜屑处理含Hg2+的废水。反应的离子方程式为 。
② 化学沉淀法:用硫化钠处理含Hg(NO3)2的废水,生成HgS沉淀。已知:
Ksp(HgS) =1.6×10-52,当废水中c(S2-)=1×10-5mol/L时,c(Hg2+)= 。
23.
 (11分)(1)甲烷是一种较高效、洁净的能源,甲烷的燃烧热大。实验测得,在常温常压下,1g CH4完全燃烧生成液态水,放出 55.6
kJ热量。则CH4燃烧的热化学方程式为
(11分)(1)甲烷是一种较高效、洁净的能源,甲烷的燃烧热大。实验测得,在常温常压下,1g CH4完全燃烧生成液态水,放出 55.6
kJ热量。则CH4燃烧的热化学方程式为
。
(2)甲烷燃料电池能量转化率较高,具有广阔的发展前景。
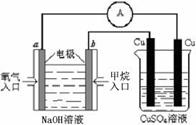 现用甲烷燃料电池进行右图所示实验:
现用甲烷燃料电池进行右图所示实验:
① 在图中标出电子的流向;
②甲烷燃料电池中,负极的电极反应式 为 ;
③ 上右图装置中,某一铜电极的质量减轻3.2 g,则a极上消耗的O2在标准状况下的体积为 L。
(3)反应一段时间后,生成的Na2CO3溶液(溶质仅为Na2CO3)中存在的关系正确的是
A.c(Na+)=c(HCO3-)=c(OH-)=c(H+) B.c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
C.c(Na+) > c(CO32-) > c(H+) > c(OH-) D.c(Na+) > c(CO32-) > c(OH-) > c(HCO3-)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com