
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
1558. МгШШNH4HCO3ЙЬЬхжС200Ёц(1)ШєНЋЛьКЯЦјЬхвРДЮЭЈЙ§Na2O2ЁЂХЈH2SO4ЃЌNa2O2діжиa1 gЃЌ
ХЈH2SO4діжиb1 g(2)ШєНЋЛьКЯЦјЬхвРДЮЭЈЙ§ХЈH2SO4ЁЂNa2O2ЃЌдђХЈH2SO4діжиb2 gЃЌNa2O2
діжиa2 gЃЌ(УПДЮЭЈЙ§ЦјЬхЪБГфЗжЗДгІ)дђa1ЁЂa2ЁЂb1ЁЂb2ДгДѓЕНаЁЕФЫГађЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
1556ЁЂЯТСаЮяжЪжаЦфаджЪгыгУЭОВЛЯрЗћЕФЪЧ(ЁЁЁЁ )
AЁЂNa2O2ЃКгУзїЦЏАзМСЁЁЁЁЁЁ BЁЂNa - KКЯН№ЃКгУгкдзгЗДгІЖбЕФЕМШШМСЁЁЁЁЁЁЁЁЁЁЁЁ CЁЂNaHCO3ЃКЪГЦЗЗЂНЭМСЁЁЁЁЁЁЁЁ DЁЂNa2CO3ЃКжЮСЦЮИЫсЙ§Жр
 ЁЁ
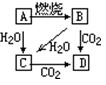
1557. гвЭМAЪЧЕЅжЪЃЌBЕФбцЩЋЗДгІГЪЛЦЩЋ
ЁЁ
1557. гвЭМAЪЧЕЅжЪЃЌBЕФбцЩЋЗДгІГЪЛЦЩЋ
ХаЖЯABCDЕФЛЏбЇЪНA_____B____C____D____
1555ЁЂЙигкяЎЕФНсЙЙКЭаджЪЕФХаЖЯЃЌДэЮѓЕФЪЧ(ЁЁЁЁ )
ЂйгыЫЎЗДгІБШФЦОчСв ЂкЫќЕФдзгАыОЖБШФЦаЁ ЂлЫќЕФбѕЛЏЮяБЉТЖдкПеЦјжавзЮќЪеЖўбѕЛЏЬМ ЂмЫќЕФбєРызгЕФзюЭтВуЕчзгЪ§КЭФЦЕФЯрЭЌ ЂнЫќЪЧЛЙдМС
AЁЂЂйЂмЁЁЁЁ BЁЂЂкЂлЁЁЁЁ CЁЂЂлЂнЁЁЁЁ DЁЂЂй
1554. ЕБФЦШМЩеЪБЃЌзюЪЪвЫУ№Л№ЕФЪЧ(ЁЁЁЁ )
ЁЁЁЁ AЁЂХнФУ№Л№ЦїЁЁЁЁЁЁЁЁ BЁЂвКЬЌCO2У№Л№Цї
ЁЁЁЁ CЁЂИЩЗлУ№Л№ЦїЁЁЁЁЁЁЁЁ DЁЂЩАЭСЁЁ
1553. Na2OгыNa2O2ЕФЙВЭЌжЎДІЪЧ(ЁЁЁЁ )
AЁЂОљЮЊАзЩЋЙЬЬхЁЁЁЁ BЁЂЖМФмгыЫЎзїгУЩњГЩМю
CЁЂОљЮЊМюадбѕЛЏЮяЁЁ DЁЂЖМФмзїУоЁЂУЋжЏЮяЕФЦЏАзМС
17.(2)ШєгУNaOH(ЙЬЬх)86g ЃЌдђжЦШЁЪБашЫЎЖрЩйПЫЃП
1552ЁЂ25ЁцЪБЃЌФЦЕФШ§жжЛЏКЯЮяЕФШмНтЖШШчЯТБэЃК
|
ЛЏКЯЮя |
NaHCO3 |
Na2CO3 |
NaOH |
|
ШмНтЖШ/g |
9 |
33 |
110 |
ИУЮТЖШЪБЃЌгУNaOHЁЂЫЎЁЂCaCO3КЭбЮЫсЮЊдСЯжЦБИВЂДгШмвКжаНсОЇГі33gДПNaHCO3 ЁЃ
(1)ШєгУЫЎ100g ЃЌдђжЦШЁЪБашNaOHЖрЩйПЫЃП
1551ЁЂ (1)вбжЊбѕЛЏЮягаЃКЦеЭЈбѕЛЏЮяЃЌШчNa2OЃЛЙ§бѕЛЏЮяЃЌШчNa2O2ЃЛГЌбѕЛЏЮяЃЌШчKO2ЃЛГєбѕЛЏЮяЃЌШчRbO3ЃЌЦфжаКѓШ§жжОљФмгыЫЎ ЛђCO2ЗДгІЩњГЩO2 ЁЃЪдЗжБ№аДГіKO2ЁЂRbO3гыCO2ЗДгІЕФЛЏбЇЗНГЬЪНЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЃ
(1)вбжЊбѕЛЏЮягаЃКЦеЭЈбѕЛЏЮяЃЌШчNa2OЃЛЙ§бѕЛЏЮяЃЌШчNa2O2ЃЛГЌбѕЛЏЮяЃЌШчKO2ЃЛГєбѕЛЏЮяЃЌШчRbO3ЃЌЦфжаКѓШ§жжОљФмгыЫЎ ЛђCO2ЗДгІЩњГЩO2 ЁЃЪдЗжБ№аДГіKO2ЁЂRbO3гыCO2ЗДгІЕФЛЏбЇЗНГЬЪНЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЃ
(2)ЯжвбгУЦНЕзЩеЦПЪеМЏЕНCO2ЃЌдкЦПФкгавЛжЛдњНєдкВЃСЇЙмФЉЖЫЕФЦјЧђЃЌШчЭМЫљЪОЁЃДђПЊШћзгбИЫйЭљЦПРяМгШыЯТСаЮяжЪжаЕФЁЁЁЁЁЁЁЁ (ЬюађКХ)ЃЌСЂМДШћНєШћзгЃЌвЛЖЮЪБМфКѓЃЌЦјЧђЛсздЖЏХђеЭЦ№РДЁЃAЁЂNa2OЁЁ BЁЂNa2O2ЁЁ CЁЂKO2ЁЁ DЁЂRbO3
1550ЁЂ
ЂйаДГіCO2гыNa2O2ЗДгІЕФЛЏбЇЗНГЬЪНЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЂкФГбЇЩњХаЖЯSO2КЭNa2O2ЗДгІФмЩњГЩСђЫсФЦЃЌФуШЯЮЊЫћЕФХаЖЯКЯРэТ№ЃПЁЁЁЁЁЁ ЁЃ
МђвЊЫЕУїРэгЩЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
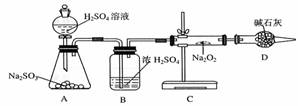
ЂлИУЭЌбЇЮоЗЈЖЯЖЈSO2КЭNa2O2ЗДгІжаЪЧЗёгабѕЦјЩњГЩЃЌФтгУЩЯЭМзАжУНјааЪЕбщЁЃ
ЁЁ (вбжЊЃКNa2SO3+2H2SO4ЁЁЁЁ Na2SO4+H2O+SO2Ёќ)
зАжУBЕФзїгУЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЛ
DЕФзїгУЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂмЮЊШЗШЯSO2КЭNa2O2ЗДгІВњЮяЃЌИУЭЌбЇЩшМЦСЫвдЯТЪЕбщВНжшЃЌЧыФуДгжаЬєбЁГіе§ШЗЕФбЁЯюВЂАДВйзїЫГађХХСа(ЬюађКХ)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ AЃЎгУДјЫЎаЧЕФФОЬѕППНќИЩдяЙмПкЃЌЙлВьФОЬѕЪЧЗёИДШМЃЛ
BЃЎгУCзАжУжаЗДгІКѓЕФЙЬЬхЮяжЪШмгкЪЪСПЫЎХфГЩШмвКЃЛ
CЃЎдкХфГЩЕФШмвКжаМгШыгУЯѕЫсЛЏЕФЯѕЫсБЕШмвКЃЌЙлВьЪЧЗёгаГСЕэЩњГЩЁЃ
DЃЎдкХфГЩЕФШмвКжаЯШМгШыбЮЫсЃЌдйМгШыТШЛЏБЕШмвК,ЙлВьЪЧЗёгаЦјХнЛђГСЕэЩњГЩЁЃ
1549ЁЂдкМюН№ЪєдЊЫиLiЁЂNaЁЂKЁЂRbЁЂCsдЊЫижаЁЃ
ЂХдзгАыОЖзюаЁЕФдЊЫидзгНсЙЙЪОвтЭМЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЃЛМюН№ЪєдЊЫидкздШЛНчжаЕФДцдкаЮЪНЪЧЁЁЁЁЁЁЁЁЁЁ (ЬюЫсЁЂМюЁЂбЮЁЂбѕЛЏЮя)ЁЃ
ЂЦНЋИїдЊЫиЕФЕЅжЪИї1.0 g ЃЌЗжБ№гы10mL ЫЎЗДгІЃЌЦфжаЗДгІзюОчСвЕФЪЧЁЁЁЁЁЁ ЁЁЃЌдкЯрЭЌзДПіЯТЃЌЩњГЩЦјЬхЕФжЪСПзюДѓЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
 ЁЁ
ЂЧМигыЫЎЗДгІЕФЛЏбЇЗНГЬЪНЮЊ(БъГіЕчзгзЊвЦЕФЗНЯђКЭЪ§ФП)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ,ЦфжабѕЛЏМСЪЧЁЁЁЁЁЁЁЁЁЁ
ЁЃ
ЁЁ
ЂЧМигыЫЎЗДгІЕФЛЏбЇЗНГЬЪНЮЊ(БъГіЕчзгзЊвЦЕФЗНЯђКЭЪ§ФП)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ,ЦфжабѕЛЏМСЪЧЁЁЁЁЁЁЁЁЁЁ
ЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com