
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
2. ЯжДњНЈЩшжаЕФТСКЯН№УХДАПђМмЃЌЦфГЩЗжПЩФмЪЧ(ЁЁ )
A. Al-AgКЯН№
B. Al-Cu-Mg-SiКЯН№
C. Al-PbКЯН№
D. БэУцЖЦЭЕФТС
1. ЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁЁЁ )
A. ЫљгаВЛатИжЖМжЛКЌгаН№ЪєдЊЫи
B. ЮвЙњСїЭЈЕФгВБвВФжЪЪЧН№ЪєЕЅжЪ
C. ЙуЖЋе§дкДђРЬЕФУїДњГСДЌЩЯДцдкДѓСПТСжЦВЭОп
D. УОКЯН№ЕФгВЖШКЭЧПЖШОљИпгкЖлУО
18. (2009ФъвјДЈЕїба)КЯГЩАБЙЄвЕЩњВњжаЫљгУЕФІС?FeДпЛЏМСЕФжївЊГЩЗжЪЧFeOЁЂFe2O3ЁЃ
(1)ФГFeOЁЂFe2O3ЛьКЯЮяжаЃЌЬњЁЂбѕЕФЮяжЪЕФСПжЎБШЮЊ4ЁУ5,ЦфжаFe2+гыFe3+ЮяжЪЕФСПжЎБШЮЊЁЁЁЁЁЁЁЁ ЁЃ
(2)ЕБДпЛЏМСжаFe2+гыFe3+ЕФЮяжЪЕФСПжЎБШЮЊ1ЁУ2ЪБЃЌЦфДпЛЏЛюадзюИпЃЌДЫЪБЬњЕФбѕЛЏЮяЛьКЯЮяжаЬњЕФжЪСПЗжЪ§ЮЊЁЁЁЁЁЁЁЁЁЁЁЁ (гУаЁЪ§БэЪОЃЌБЃСє2ЮЛаЁЪ§)ЁЃ
(3)вдFe2O3ЮЊдСЯжЦБИЩЯЪіДпЛЏМСЃЌПЩЯђЦфжаМгШыЪЪСПЬПЗлЃЌЗЂЩњШчЯТЗДгІЃК2Fe2O3+CИпЮТ4FeO+CO2ЁќЁЃ
ЮЊжЦЕУетжжЛюадзюИпЕФДпЛЏМСЃЌгІЯђ480 g Fe2O3ЗлФЉжаМгШыЬПЗлЕФжЪСПЮЊЁЁЁЁЁЁЁЁЁЁ ЁЁgЁЃ
ЕкШ§НкЁЁ гУЭОЙуЗКЕФН№ЪєВФСЯ
17. (2008ФъЩНЖЋЧрЕКФЃФт)гУЯТУцСНжжЗНЗЈПЩвджЦЕУАзЩЋЕФFe(OH)2ГСЕэЁЃ
ЗНЗЈвЛЃКгУВЛКЌFe3+ЕФFeSO4ШмвКгыгУВЛКЌO2ЕФеєСѓЫЎХфжЦЕФNaOHШмвКЗДгІжЦБИЁЃ
(1)гУСђЫсбЧЬњОЇЬхХфжЦЩЯЪіFeSO4ШмвКЪБЛЙашМгШыЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)Г§ШЅеєСѓЫЎжаШмНтЕФO2ГЃВЩгУЕФЗНЗЈЁЃ
(3)ЩњГЩАзЩЋFe(OH)2ГСЕэЕФВйзїЪЧгУГЄЕЮЙмЮќШЁВЛКЌO2ЕФNaOHШмвКЃЌВхШыFeSO4ШмвКвКУцЯТЃЌдйМЗГіNaOHШмвКЃЌетбљВйзїЕФРэгЩЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЗНЗЈЖўЃКдкШчЭМзАжУжаЃЌгУNaOHШмвКЁЂЬњаМЁЂЯЁH2SO4ЕШЪдМСжЦБИЁЃ
(1)дкЪдЙмЂёРяМгШыЕФЪдМСЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЃ
(2)дкЪдЙмЂђРяМгШыЕФЪдМСЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)ЮЊСЫжЦЕУАзЩЋFe(OH)2ГСЕэЃЌдкЪдЙмЂёКЭЂђжаМгШыЪдМСЃЌДђПЊжЙЫЎМаЃЌШћНєШћзгКѓЕФЪЕбщВНжшЪЧЁЁЁЁЁЁЁЁ ЁЃ
(4)етбљЩњГЩЕФFe(OH)2ГСЕэФмНЯГЄЪБМфБЃГжАзЩЋЃЌЦфРэгЩЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
16. (ЛЏбЇТГПЦБиао1 P59ЃЌ3Ьт)ЕчзгЙЄвЕГЃгУ30%ЕФFeCl3ШмвКИЏЪДЗѓдкОјдЕАхЩЯЕФЭВЃЌжЦдьгЁЫЂЕчТЗАхЁЃ
(1)МьбщШмвКжаFe3+ДцдкЕФЪдМСЪЧЁЁЁЁЁЁЁЁ ЃЌжЄУїFe3+ДцдкЕФЯжЯѓЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)аДГіFeCl3ШмвКгыН№ЪєЭЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)ФГЙЄГЬЪІЮЊСЫДгЪЙгУЙ§ЕФИЏЪДЗЯвКжаЛиЪеЭЃЌВЂжиаТЛёЕУFeCl3ШмвКЃЌзМБИВЩгУЯТСаВНжшЃК

A. ЧыаДГіЩЯЪіЪЕбщжаМгШыЛђЩњГЩЕФгаЙиЮяжЪЕФЛЏбЇЪНЃК
ЂйЁЁЁЁЁЁЁЁ ЃЌЂкЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌЂлЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌЂмЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЃЌ
ЂнЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌЂоЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
B. ЧыаДГіЯрЙиЗДгІЕФЛЏбЇЗНГЬЪН: ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
15. (2009ФъИпПМНЫеОэ)вдТШЛЏМиКЭюбАзГЇЕФИБВњЦЗСђЫсбЧЬњЮЊдСЯЩњВњСђЫсМиЁЂЙ§ЖўСђЫсяЇКЭбѕЛЏЬњКьбеСЯЃЌдСЯЕФзлКЯРћгУТЪНЯИпЁЃЦфжївЊСїГЬШчЯТЃК
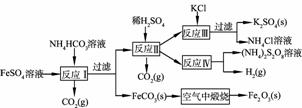
(1)ЗДгІЂёЧАашдкFeSO4ШмвКжаМгШыЁЁЁЁЁЁЁЁ (ЬюзжФИ)ЃЌвдГ§ШЅШмвКжаЕФFe3+ЁЃ
A. аПЗлB. ЬњаМC. KIШмвКD. H2
(2)ЗДгІЂёашПижЦЗДгІЮТЖШЕЭгк35 ЁцЃЌЦфФПЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)ЙЄвЕЩњВњЩЯГЃдкЗДгІЂѓЕФЙ§ГЬжаМгШывЛЖЈСПЕФДМРрШмМСЃЌЦфФПЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(4)ЗДгІЂєГЃБЛгУгкЕчНтЩњВњ(NH4)2S2O8(Й§ЖўСђЫсяЇ)ЁЃЕчНтЪБОљгУЖшадЕчМЋЃЌбєМЋЗЂЩњЕФЕчМЋЗДгІПЩБэЪОЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
14. (2009ФъИпПМББОЉОэЁЄРэзл)вдИЛКЌСђЫсбЧЬњЕФЙЄвЕЗЯвКЮЊдСЯЩњВњбѕЛЏЬњЕФЙЄвеШчЯТ(ВПЗжВйзїКЭЬѕМўТд)ЃК
ЂёДгЗЯвКжаЬсДПВЂНсОЇГіFeSO4ЁЄ7H2O
ЂђНЋFeSO4ЁЄ7H2OХфжЦГЩШмвК
ЂѓFeSO4ШмвКгыЩдЙ§СПЕФNH4HCO3ШмвКЛьКЯЃЌЕУЕНКЌFeCO3ЕФзЧвК
ЂєНЋзЧвКЙ§ТЫЃЌгУ90 ЁцШШЫЎЯДЕгГСЕэЃЌИЩдяКѓЕУЕНFeCO3ЙЬЬх
ЂѕьбЩеFeCO3ЃЌЕУЕНFe2O3ЙЬЬх
вбжЊЃКNH4HCO3дкШШЫЎжаЗжНтЁЃ
(1)ЂёжаЃЌМгзуСПЕФЬњаМГ§ШЅЗЯвКжаЕФFe3+ЃЌИУЗДгІЕФРызгЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)ЂђжаЃЌашМгвЛЖЈСПСђЫсЃЌдЫгУЛЏбЇЦНКтдРэМђЪіСђЫсЕФзїгУЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)ЂѓжаЃЌЩњГЩFeCO3ЕФРызгЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ШєFeCO3зЧвКГЄЪБМфБЉТЖдкПеЦјжаЃЌЛсгаВПЗжЙЬЬхБэУцБфЮЊКжЩЋЃЌИУБфЛЏЕФЛЏбЇЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁ ЁЃ
(4)ЂєжаЃЌЭЈЙ§МьбщSO2-4РДХаЖЯГСЕэЪЧЗёЯДЕгИЩОЛЃЌМьбщSO2-4ЕФВйзїЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(5)вбжЊьбЩеFeCO3ЕФЛЏбЇЗНГЬЪНЪЧ4FeCO3+O2ИпЮТ2Fe2O3+4CO2,ЯжьбЩе464.0 kgЕФFeCO3,ЕУЕН316.8 kgВњЦЗЃЌШєВњЦЗжадгжЪжЛгаFeOЃЌдђИУВњЦЗжаFe2O3ЕФжЪСПЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ kgЁЃ(ФІЖћжЪСП/gЁЄmol-1;ЁЁ FeCO3:116ЁЁ Fe2O3:160ЁЁ FeO:72)
13. гЩЬњКЭбѕЛЏЬњзщГЩЕФЛьКЯЮягыЯЁH2SO4зїгУЃЌЙЬЬхЧЁКУШмНтЃЌЫљЕУШмвКжаВЛКЌFe3+ЃЌЧвЩњГЩЕФFe2+гыH2ЕФЮяжЪЕФСПжЎБШЮЊ4ЁУ1ЁЃдђЗДгІЮяжаFe2O3ЁЂFeЁЂH2SO4ЕФЮяжЪЕФСПжЎБШЮЊЁЁЁЁЁЁЁЁ ЁЃ
12. ШЁ14.4 gВнЫсбЧЬњ(FeC2O4)ЃЌИєОјПеЦјМгШШЗжНтЃЌНсЙћЕУЕН7.2 gЬњЕФбѕЛЏЮяЃЌДЫбѕЛЏЮягІЪЧ(ЁЁ )
A. Fe2O3
B. FeO
C. Fe3O4
D. FeOЁЄFe3O4
11. (2009ФъЩНЖЋСйвЪФЃФт)ФГЯЁШмвКжаКЌгаFe(NO3)3ЁЂCu(NO3)2ЁЂHNO3,ШєЯђЦфжаж№НЅМгШыЬњЗлЃЌШмвКжаFe2+ХЈЖШКЭМгШыЬњЗлЕФЮяжЪЕФСПжЎМфЕФЙиЯЕШчЭМЫљЪОЃЌдђЯЁШмвКжаFe(NO3)3ЁЂCu(NO3)2ЁЂHNO3ЮяжЪЕФСПХЈЖШжЎБШЮЊ()
A. 1ЁУ1ЁУ1B. 1ЁУ3ЁУ1ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
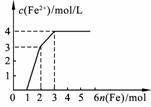
C. 3ЁУ3ЁУ8D. 1ЁУ1ЁУ4ЁЁЁЁЁЁ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com