
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
15. ЧІаюЕчГиЪЧЛЏбЇЕчдДЃЌЫќЙЄзїЪБЕФЕчГизмЗДгІЮЊЃКPbO2+Pb+2H2SO4=2PbSO4+2H2OЁЃЪдЛиД№ЃК
(1)аюЕчГиИКМЋЕФЕчМЋВФСЯЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)ЙЄзїЪБИУаюЕчГие§МЋЕФЕчМЋЗДгІЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЃ
(3)ЧІаюЕчГиЙЄзїЪБЃЌЕчНтжЪШмвКЕФУмЖШЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЁАМѕаЁЁБЁЂЁАдіДѓЁБЛђЁАВЛБфЁБЃЌЯТЭЌ)ЃЌpHЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(4)ШчЙћгУЧІаюЕчГизїЕчдДЕчНтБЅКЭЪГбЮЫЎжЦШЁCl2ЃЌЕБжЦЕУ0.05 molЁЁ Cl2ЪБЃЌдкРэТлЩЯЕчГиФкВПЯћКФЕФH2SO4ЕФЮяжЪЕФСПЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
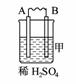
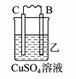
14. гЩAЁЂBЁЂCЁЂDЫФжжН№ЪєАДЯТБэжазАжУЭМНјааЪЕбщЁЃ
|
ЁЁ зАжУ |
 |
 |
 |
|
ЯжЯѓ |
ЖўМлН№ЪєA ВЛЖЯШмНт |
CЕФжЪСП діМг |
AЩЯгаЦј ЬхВњЩњ |
ИљОнЪЕбщЯжЯѓЛиД№ЯТСаЮЪЬтЃК
(1)зАжУМзжаИКМЋЕФЕчМЋЗДгІЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)зАжУввжае§МЋЕФЕчМЋЗДгІЪНЪЧЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(3)зАжУБћжаШмвКЕФpHЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЁАБфДѓЁБЁЂЁАБфаЁЁБЛђЁАВЛБфЁБ)ЁЃ
(4)ЫФжжН№ЪєЛюЦУадгЩЧПЕНШѕЕФЫГађЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
13. (2009ФъИпПМИЃНЈОэ)ПижЦЪЪКЯЕФЬѕМўЃЌНЋЗДгІ2Fe3++2I-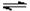 2Fe2++I2ЩшМЦГЩШчЭМЫљЪОЕФдЕчГиЁЃЯТСаХаЖЯВЛе§ШЗЕФЪЧ(ЁЁ )
2Fe2++I2ЩшМЦГЩШчЭМЫљЪОЕФдЕчГиЁЃЯТСаХаЖЯВЛе§ШЗЕФЪЧ(ЁЁ )
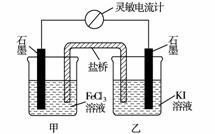
A.ЗДгІПЊЪМЪБЃЌввжаЪЏФЋЕчМЋЩЯЗЂЩњбѕЛЏЗДгІ
B.ЗДгІПЊЪМЪБЃЌМзжаЪЏФЋЕчМЋЩЯFe3+БЛЛЙд
C.ЕчСїМЦЖСЪ§ЮЊСуЪБЃЌЗДгІДяЕНЛЏбЇЦНКтзДЬЌ
D.ЕчСїМЦЖСЪ§ЮЊСуКѓЃЌдкМзжаШмШыFeCl2ЙЬЬхЃЌввжаЪЏФЋЕчМЋЮЊИКМЋ
12. (2007ФъИпПМЙуЖЋОэЁЄЮФЛљ)ЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁ )
A.ашвЊМгШШЕФЛЏбЇЗДгІЖМЪЧЮќШШЗДгІ
B.жаКЭЗДгІЖМЪЧЗХШШЗДгІ
C.дЕчГиЪЧНЋЕчФмзЊЛЏЮЊЛЏбЇФмЕФвЛжжзАжУ
D.ЫЎСІЗЂЕчЪЧНЋЛЏбЇФмзЊЛЏЮЊЕчФмЕФЙ§ГЬ
11. (2007ФъИпПМЙуЖЋОэ)ИжЬњдкГБЪЊЕФПеЦјжаЛсБЛИЏЪДЃЌЗЂЩњЕФдЕчГиЗДгІЮЊЃК2Fe+2H2O+O2=2Fe2++4OH-вдЯТЫЕЗЈе§ШЗЕФЪЧ(ЁЁ )
A.ИКМЋЗЂЩњЕФЗДгІЮЊЃКFe-2e-=Fe2+
B.е§МЋЗЂЩњЕФЗДгІЮЊЃК2H2O+O2+2e-=4OH-
C.дЕчГиЪЧНЋЕчФмзЊБфЮЊЛЏбЇФмЕФзАжУ
D.ИжжљдкЫЎЯТВПЗжБШПеЦјгыЫЎНЛНчДІИќШнвзИЏЪД
10. вЛжжаТаЭШМСЯЕчГиЃЌЫќЪЧгУСНИљЖшадН№ЪєзіЕчМЋВхШыKOHШмвКжаЃЌШЛКѓЯђСНМЋЩЯЗжБ№ЭЈШыМзЭщКЭбѕЦјЃЌЗЂЩњЕФЕчМЋЗДгІЮЊЃК
XМЋЃКCH4+10OH--8e-=CO32-+7H2O
YМЋЃК4H2O+2O2+8e-=8OH-
ЙигкДЫШМСЯЕчГиЕФЯТСаЫЕЗЈжаДэЮѓЕФЪЧ(ЁЁ )
A.XМЋЮЊИКМЋЃЌYМЋЮЊе§МЋ
B.ЙЄзївЛЖЮЪБМфКѓЃЌKOHЕФЮяжЪЕФСПМѕЩй
C.дкБъзМзДПіЯТЭЈШы5.6 L O2ЭъШЋЗДгІЃЌдђга1.0 mol ЕчзгЗЂЩњзЊвЦ
D.ИУЕчГиЙЄзїЪБМзЭщвЛМЋИННќШмвКЕФpHЩ§Ип
9. ЯТЭМЮЊЧтбѕШМСЯЕчГидРэЪОвтЭМЃЌАДееДЫЭМЕФЬсЪОЃЌЯТСаа№ЪіВЛе§ШЗЕФЪЧ(ЁЁ )
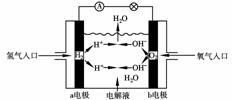
A.aЕчМЋЪЧИКМЋ
B.bЕчМЋЕФЕчМЋЗДгІЮЊЃК4OH--4e-=2H2O+O2Ёќ
C.ЧтбѕШМСЯЕчГиЪЧвЛжжОпгагІгУЧАОАЕФТЬЩЋЕчдД
D.ЧтбѕШМСЯЕчГиЪЧвЛжжВЛашвЊНЋЛЙдМСКЭбѕЛЏМСШЋВПДЂВидкЕчГиФкЕФаТаЭЗЂЕчзАжУ
8. (2007ФъИпПМШЋЙњОэЂђ)дкЪЂгаЯЁH2SO4ЕФЩеБжаЗХШыгУЕМЯпСЌНгЕФаПЦЌКЭЭЦЌЃЌЯТСаа№Ъіе§ШЗЕФЪЧ(ЁЁ )
A.е§МЋИННќЕФSO42-РызгХЈЖШж№НЅдіДѓ
B.ЕчзгЭЈЙ§ЕМЯпгЩЭЦЌСїЯђаПЦЌ
C.е§МЋгаO2внГі
D.ЭЦЌЩЯгаH2внГі
7. МюадЕчГиОпгаШнСПДѓЁЂЗХЕчЕчСїДѓЕФЬиЕуЃЌвђЖјЕУЕНЙуЗКгІгУЁЃаПУЬМюадЕчГивдЧтбѕЛЏМиШмвКЮЊЕчНтвКЃЌЕчГизмЗДгІЪНЮЊZn(s)+2MnO2(s)+2H2O(l)=Zn(OH)2(s)+2MnOOH(s)
ЯТСаЫЕЗЈДэЮѓЕФЪЧ(ЁЁ )
A.ЕчГиЙЄзїЪБЃЌаПЪЇШЅЕчзг
B.ЕчГие§МЋЕФЕчМЋЗДгІЪНЮЊ2MnO2(s)+2H2O(l)+2e-=2MnOOH(s)+2OH-(aq)
C.ЕчГиЙЄзїЪБЃЌЕчзггЩе§МЋЭЈЙ§ЭтЕчТЗСїЯђИКМЋ
D.ЭтЕчТЗжаУПЭЈЙ§0.2 molЕчзгЃЌаПЕФжЪСПРэТлЩЯМѕЩй6.5 g
6. НЋНрОЛЕФН№ЪєЦЌМзЁЂввЁЂБћЁЂЖЁЗжБ№ЗХжУдкНўгаФГжжбЮШмвКЕФТЫжНЩЯУцВЂбЙНє(ШчЭМЫљЪО)ЁЃдкУПДЮЪЕбщЪБЃЌМЧТМЕчбЙБэжИеыЕФЦЋзЊЗНЯђКЭЕчбЙБэЕФЖСЪ§ШчЯТБэЃК
|
Н№Ъє ЁЁ |
ЕчзгСїЖЏЗНЯђ |
ЕчбЙ/V ЁЁ |
|
Мз |
МзЁњCu |
+0.78ЁЁ |
|
вв |
CuЁњвв |
-0.15 |
|
Бћ |
БћЁњCu |
+1.35 |
|
ЖЁ |
ЖЁЁњCu |
+0.30 |
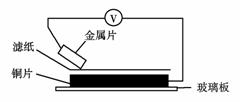
ЧывРОнМЧТМЪ§ОнХаЖЯЃЌЯТСагаЙиЫЕЗЈе§ШЗЕФЪЧ(ЁЁ )
A.дкЫФжжН№ЪєжаввЕФЛЙдадзюЧПЁЁ
B.Н№ЪєввФмДгСђЫсЭШмвКжажУЛЛГіЭ
C.МзЁЂЖЁШєаЮГЩдЕчГиЪБЃЌМзЮЊе§МЋ
D.МзЁЂвваЮГЩКЯН№ЪБЃЌНЋИУКЯН№ТЖжУдкПеЦјжаЃЌМзЯШБЛИЏЪД
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com