
题目列表(包括答案和解析)
23.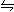 恒温恒压下,在一个可变容积的容器中发生如下反应:3A(g)+B(g) 2C(g)
恒温恒压下,在一个可变容积的容器中发生如下反应:3A(g)+B(g) 2C(g)
(1)若开始时放入3molA(g)和1molB(g),达到平衡后,生成amolC(g),这时A的物质的量为
mol。(用含a的式子来表示,下同)
(2)若开始时,放入1.5molA(g),0.5molB(g),达到平衡时,生成C的物质的量为 mol。
(3)若开始时,放入xmolA(g),2molB(g)和2molC(g),达到平衡后,A和C的物质的量分别为ymol和3amol,则x= mol,y= mol。
(4)若维持温度不变,在一个与(1)反应前起始体积相同且容积固定的容器中发生上述反应。
开始3molA(g)和lmolB(g),达到平衡后生成bmolC(g),则a和b的关系是: ,理由是 。

22.(14分)农村中秸杆的综合利用不仅可以提高经济效益,为农民创收,而且还能防止环境污染。现按下列方式处理:
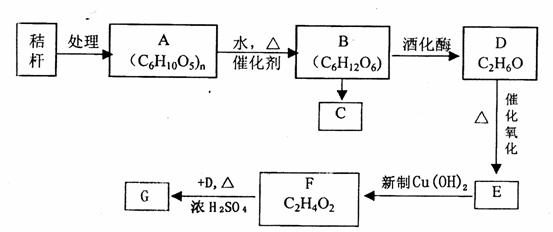
已知G是具有香味的液体,请回答:
 (1)F G的化学方程式:
;
(1)F G的化学方程式:
;
 E F的化学方程式:
o
E F的化学方程式:
o
(2)已知C中含碳、氢、氧,质量分数分别为40.0%、6.67%、53.3%,其碳原子为B的一半,则C的分子式为 。
(3)与G的分子式相同,其中含有 结构的链状同分异构体最多有 种(不包括G),写出属于不同于G种类的两种同分异构体的结构简式:
.
结构的链状同分异构体最多有 种(不包括G),写出属于不同于G种类的两种同分异构体的结构简式:
.
21.(11分)食盐是日常生活的必需品,也是重要的化工原料。
⑴粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、S042-等杂质离子,实验室提纯NaCl的流程
如下:
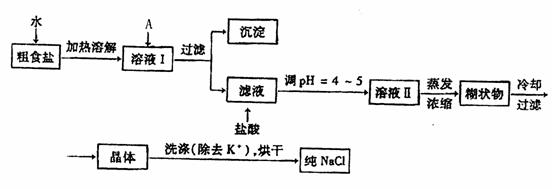
提供的试剂:饱和Na2C03溶液 饱和K2C03溶液 NaOH溶液 BaCl2溶液 Ba(NO3)2溶液 75%乙醇 四氯化碳
①欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、S042-离子,选出A所代表的试剂,按滴加顺序依次为
(只填化学式)。
②洗涤除去NaCl晶体表面附带的少量KCl,所选用的试剂为以上提供试剂中的75%乙醇,
 请说明原因
o
请说明原因
o
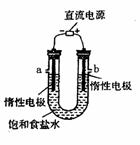
⑵电解饱和食盐水的装置如图所示,若收集的H2为2L。则同样条件下收集的C12 (填“>”、“=”或“<”)2L,原因是 。
装置改进后,可用于制备NaOH溶液,若测定溶液中NaOH的浓度,常用的方法为 。装置a口出来的气体是 。写出该装置中发生的电解反应方程式 。
20.(15分)如下图所示是电子工业中某原料的生产流程,其中反应②③是你在课本习题中见过,其目的是为了提纯B;物质A-H均为短周期元素组成;G为五原子非极性分子;A-D均是单质且元素原子的最外层电子数目的关系为C>A=B>D;H极易溶于水,且其水溶液为-种强酸。
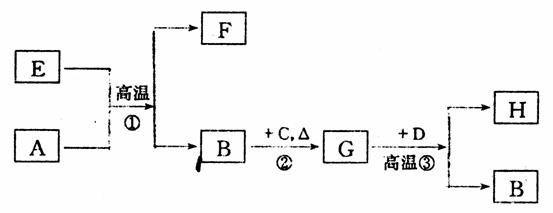
请回答下列问题:
(1)B的电子排布式: ;固体E的晶体类型 ;H中的键型为 (填“π”或“δ”);
(2)反应①的化学方程式: 。
(3)与反应①类型相同,且两种单质分属同一主族和不同主族的反应,用化学方程式各写- 例:
①单质属同-主族: ;
②单质属不同主族: o
(4)F在工业上有多种用途,写出其中一种用途的化学方程式:
19.(7分)某反应体系中的物质有:A1203、AlN、C、N2、C02
(1)请将A1203之外的反应物和生成物分别填入以下空格中
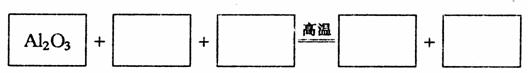
(2)当体系中有6mol还原剂被氧化时,转移 mol电子
(3)氮化铝(A1N)广泛应用于电子、陶瓷等工业领域,在甘定条件下,可发生水解,请写出其水解方程式: 。
18.将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应:
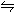 H2(g)+Br2(g) 2HBr(g) △H<0
H2(g)+Br2(g) 2HBr(g) △H<0
平衡时,H2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时,H2(g)的转化率为b,a和b的关系是 ( )
A.a=b B.a<b C.a>b D.无法确定
第Ⅱ卷 非选择题(共59分)
17.某温度时,BaS04在水中的沉淀平衡曲线如图所
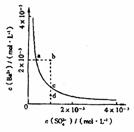 示。下列说法正确的是
示。下列说法正确的是
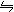 提示:BaS04(s) Ba2+(aq)十S042- (aq)的平衡常数
提示:BaS04(s) Ba2+(aq)十S042- (aq)的平衡常数
Ksp=c(Ba2+)·c(S042-)称为溶度积常数 ( )
A.加入Na2SO4可以使溶液由a点变到b点
B.通过蒸发可以使溶液由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
16.-定体积的某物质的水溶液,其质量分数为30%,当加入等体积的水稀释后,质量分数大于15%,则原溶液的密度 ( )
A.小于水的密度 B.大于水的密度 C.等于水的密度 D.无法确定
14,研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到直观形象的效果,下列表达不正确的是: ( )
A.Na0H溶液与SO2反应时溶液中的学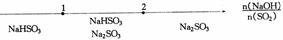
B.NaNO2溶液与盐酸反应后铝的存在形式


15.下列各溶液中,微粒的物质的量浓度关系不正确的是 ( )
A.10mL0.5mol·L-1CH3COONa溶液和6ml的1mol·L-l盐酸混合
c(C1-)>c(Na+)>c(H+)>c(OH-)
B.0.1mol·L-1pH=4的NaHB溶液中 c(Na+)>c(HB-)>c(H2B)>c(B2-)
C.在NaHA溶液中一定有 c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-)
D.在c(NH4Cl)相等的NH4C1、(NH4)2S04、(NH4)2C03三种溶液中
c(NH4C1)>c[(NH4)2C03]>c[(NH4)2S04]
13.灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
①Sn(s,白)+2HCl(aq)=SnCl2(aq)+H2(g) △Hl
②Sn(s,灰)+2HCI(aq)=SnCl2(aq)+H2(g) △H2
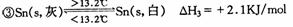
下列说法正确的是 ( )
A.△Hl>△H2
B.灰锡转化为白锡的反应是放热反应
C.锡在常温下以灰锡状态存在
D.锡制器皿长期处于低于13.2℃的环境中,会自行毁坏
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com