
题目列表(包括答案和解析)
1.X、Y、Z、M是4种短周期元素,其中X、Y位于同一主族,Y与M、X与Z位于同一周期。X原子最外层电子数是其电子层数的3倍。Z原子的核外电子数比X原子少1。M是同周期中原子半径最大的元素(除稀有气体元素外)。下列说法正确的是( )
A.Y元素最高价氧化物对应水化物的化学式可表示为HYO3
B.Z和M组成的化合物为离子化合物,它与盐酸反应可以生成两种盐
C.X、Y、Z元素的气态氢化物中,Y的沸点最高
D.四种元素简单离子的半径由大到小依次为Y>Z>X>M
解析:由X原子最外层电子数是其电子层数的3倍推出X是O元素,由X、Y位于同一主族,推出Y是S元素,由Z原子的核外电子数比X原子少1,推出Z是N元素,Y与M同周期,且M是同周期中原子半径最大的元素(除稀有气体元素外),故M是Na元素。A项,Y元素即S元素,其最高价氧化物对应水化物的化学式为H2SO4;B项,Z、M形成的化合物为Na3N,与盐酸反应生成NaCl、NH4Cl两种盐,正确;C项,X、Y、Z元素的气态氢化物中,X(H2O)的沸点最高;D项,四种元素简单离子中S2-半径最大,Na+、O2-、N3-电子层结构相同,原子序数越大,离子半径越小,故正确。
答案:BD
13.A、B、C、D、E、F、G都是短周期主族元素,它们的核电荷数依次增大。元素A的原子核内仅有一个质子,A、D同主族,B、C为同周期元素且与A能形成相同电子数的化合物,C与F同主族,F的质子数为C的2倍,元素E的最外层电子数比K层电子数多1,B、C、F的质子数之和等于E、G的质子数之和。请回答下列问题:
(1)写出由上述至少两种元素组成的具有漂白作用的物质的化学式________________(至少写出四种)。
(2)A分别与B、C、G能形成相应的最常见三种化合物,这三种化合物的沸点由高到低的顺序为______________(用化学式表示)。
(3)由A、B、C、D四种元素组成的一种常见化合物的溶液分别与由A、C、D、E四种元素组成的一种化合物的溶液和由E、G两种元素组成的一种化合物的溶液都能反应得到同一种白色沉淀,写出上述两个反应的离子方程式________________、________________。
(4)D、E两种元素的原子都能形成相应的离子,则两离子半径大小关系为________________(用离子符号表示);将D、E两种元素的单质同时投入水中,充分反应后,测得溶液中只有一种溶质,且无固体物质剩余,则所投入到水中的D的单质和E的单质的质量之比为________,上述反应的化学方程式为________________;若D的单质的物质的量为x mol,则上述反应中得到另一物质的物质的量为________。
解析:根据题设条件可推知A为H、B为C、C为O、D为Na、E为Al、F为S、G为Cl。
(1)H2O2、Na2O2、NaClO、HClO、SO2等均具有漂白性。
(2)由于H2O分子间存在氢键,其沸点高于HCl、CH4,又由于HCl的相对分子质量大于CH4,HCl的沸点高于CH4,故沸点由高到低的顺序为:H2O>HCl>CH4。
(3)A、B、C、D四种元素组成的化合物为NaHCO3,HCO能分别与[Al(OH)4]-和Al3+反应生成Al(OH)3沉淀,其相关反应的离子方程式为:HCO+[Al(OH)4]-===CO+Al(OH)3↓+H2O,3HCO+Al3+===Al(OH)3↓+3CO2↑。
(4)Al3+和Na+有相同的电子层结构,根据具有相同电子层结构的微粒,其原子序数越小离子半径越大,可得r(Na+)>r(Al3+)。Na首先与H2O反应生成NaOH:2Na+2H2O===2NaOH+H2↑,Al再与NaOH反应刚好生成NaAlO2:2Al+2NaOH+2H2O===2NaAlO2+3H2↑,其总反应式为:Na+Al+2H2O===NaAlO2+2H2↑,故参与反应的Na、Al的质量比为23∶27。反应得到H2的物质的量为Na的2倍,即为2x mol。
答案:(1)SO2、Na2O2、HClO、NaClO(其他合理答案均可) (2)H2O>HCl>CH4 (3)HCO+[Al(OH)4]-+H2O===CO+Al(OH)3↓ 3HCO+Al3+===Al(OH)3↓+3CO2↑
(4)r(Na+)>r(Al3+) 23∶27 Na+Al+4H2O===Na[Al(OH)4]+2H2↑ 2x mol
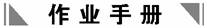
12. (2008·海南,14)根据元素周期表1-20号元素的性质和递变规律,回答下列问题。
(1)属于金属元素的有__________种,金属性最强的元素与氧反应生成的化合物有____________(填两种化合物的化学式);
(2)属于稀有气体的是__________(填元素符号,下同);
(3)形成化合物种类最多的两种元素是_________________________________________;
(4)第三周期中,原子半径最大的是(稀有气体除外)_________________________________;
(5)推测Si、N最简单氢化物的稳定性:____________强于__________(填化学式)。
解析:(1)1-20号元素有Li、Na、K、Ca、Al、Be和Mg共7种金属元素,金属性最强的为K,K和O2可以生成K2O、KO2、K2O2等。
(2)属于稀有气体的是He、Ne、Ar三种。
(3)形成化合物种类最多的两种元素是碳和氢。
(4)同一周期元素中,从左到右半径越来越小,因此第三周期中半径最大的元素是Na。
(5)由于N的非金属性比Si强,因此NH3比SiH4稳定。
答案:(1)7 K2O、K2O2、KO2(任选2个) (2)He、Ne、Ar (3)C、H (4)Na (5)NH3 SiH4
11.A、B、C、D、E、F六种短周期主族元素,原子序数依次增大。其中B的单质在常温下为双原子分子,它与A的单质可形成分子X,X的水溶液呈碱性;D的简单阳离子与X具有相同电子数,且D是同周期中简单离子半径最小的元素;E元素的原子最外层比次外层少两个电子,C、F两种元素的原子最外层共有13个电子。则
(1)B的原子结构示意图_____________________________________________________;
(2)B、C、E分别与A形成的化合物中最稳定的是________(写化学式);
(3)C与D形成的化合物的化学式是__________,它的性质决定了它在物质的分类中应属于________;请写出该化合物的水化物的电离方程式_________________________________;
(4)F的单质在反应中常作____________剂,该单质的水溶液与E的低价氧化物反应的离子方程式为______________________________________________________________。
解析:根据X的水溶液显碱性和A的原子序数比B小,得到B为N,A为H;D的简单阳离子为10e-结构,且在同周期简单离子中半径最小,推出D为Al元素;E的次外层电子数必须大于2,则E的核外电子排布为 ,E为S元素;F的原子序数比E大且为短周期主族元素,F只能是Cl元素,即可推出C为O元素;其余可迎刃而解。
,E为S元素;F的原子序数比E大且为短周期主族元素,F只能是Cl元素,即可推出C为O元素;其余可迎刃而解。
答案:(1)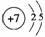 (2)H2O (3)Al2O3 两性氧化物 Al(OH)3+H2O
(2)H2O (3)Al2O3 两性氧化物 Al(OH)3+H2O [Al(OH)4]-+H+ Al(OH)3
[Al(OH)4]-+H+ Al(OH)3 Al3++3OH- (4)氧化 SO2+Cl2+2H2O===4H++SO+2Cl-
Al3++3OH- (4)氧化 SO2+Cl2+2H2O===4H++SO+2Cl-
10.下图是元素周期表前四周期的一部分,下列对相关元素的叙述正确的是( )
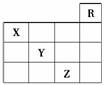
①X元素的原子有二个电子层,处于周期表的第15个纵行 ②Z的原子序数为31,单质常温下为液体 ③气态氢化物水溶液的酸性X<Y<Z ④X的气态氢化物与Y的最高价氧化物的水化物能反应生成盐 ⑤Z的原子序数比Y大19,Y的原子序数比X大9
A.只有② B.只有①③④⑤ C.只有①②③④ D.全部
解析:周期表共18个纵行,因已知是前四周期,R元素显然是He,在第18列,所以①正确;各周期元素数分别为2,8,8,18,所以Z右边的稀有气体原子序数为36,Z应该为35号,故②错;根据主族元素的分布知识,三种元素为X-氮,Y-硫,Z-溴,酸性NH3<H2S<HBr,所以③正确;NH3与H2SO4反应生成(NH4)2SO4,故④正确;同主族相邻元素原子序数之差,2、3两周期间为8,3、4两周期间从第13列开始相差为18,故⑤正确。
答案:B
9.下列有关元素性质的递变规律不正确的是( )
A.Na、Mg、Al的还原性逐渐减弱
B.HCl、PH3、H2S气态氢化物的稳定性逐渐减弱
C.NaOH、KOH的碱性逐渐增强
D.Na、K、Rb的原子半径依次增大
解析:注意结构与性质之间的关系。Na、Mg、Al电子层数相同,按原子序数递增排列,原子半径逐渐减小,核对外层电子的引力逐渐增大,失电子能力逐渐减弱,金属还原性逐渐减弱,A正确;P、S、Cl是电子层数相同,按原子序数递增排列,原子半径逐渐减小,核对外层电子的引力逐渐增大,得电子能力逐渐增强,非金属性逐渐增强,气态氢化物稳定性逐渐增强,B不正确;Na、K、Rb电子层数依次增多排列,原子半径依次增大,核对外层电子引力依次减小,失电子能力依次增强,金属性增强,NaOH、KOH碱性逐渐增强,C、D正确。
答案:B
8. 运用元素周期律分析下面的推断,其中错误的是( )
A.铍(Be)的氧化物的水化物可能具有两性
B.砹(At)为有色固体;HAt不稳定;AgAt感光性很强,且不溶于水也不溶于稀酸
C.硫酸锶(SrSO4)是难溶于水的白色固体
D.硒化氢(H2Se)是无色、有毒、比H2S稳定的气体
解析:Be、BeO、Be(OH)2均有两性;根据卤素及其化合物的递变性知,B正确;MgSO4、CaSO4、SrSO4溶解度依次减小。
答案:D
7. 下列推断正确的是( )
A.根据同浓度的两元素含氧酸钠盐(正盐)溶液的碱性强弱,可判断该两元素非金属性的强
弱
B.根据同主族两非金属元素氢化物沸点高低,可判断该两元素非金属性的强弱
C.根据相同条件下两主族金属单质与水反应的难易,可判断两元素金属性的强弱
D.根据两主族金属元素原子最外层电子数的多少,可判断两元素金属性的强弱
解析:元素非金属性的强弱与最高价含氧酸的酸性强弱对应,A错;氢化物沸点高低与元素的非金属性强弱没有必然联系,B错;当电子层数相同时,才可以根据最外层电子数的多少判断金属性的强弱,D错。
答案:C
6.A、B、C、D、E五种元素从左向右按原子序数递增(原子序数为5个连续的自然数)的顺序排列如下:
|
A |
B |
C |
D |
E |
下列说法正确的是( )
A.E元素的最高化合价为+7价时,D元素的负化合价可为-2价
B.A(OH)n为强碱时,B(OH)m也一定为强碱
C.HnDOm为强酸时,E的非金属性一定很强
D.HnCOm为强酸时,E的单质可能有强还原性
解析:E元素的最高化合价为+7价时,D元素的最高化合价必为+6价,则D元素的负化合价可为-2价;A(OH)n为强碱时,B(OH)m可能为强碱,也可能为中强碱,还可能为弱碱;HnDOm为强酸,即D元素的非金属性很强,原子序数比D大1的E可能为非金属性比D强的非金属元素,也可能为稀有气体元素;元素C与元素E的关系可这样举例如:C是16S,则E是18Ar;C是17Cl,则E是19K。
答案:AD
5.(2008·江苏,7)下列排列顺序正确的是( )
①热稳定性:H2O>HF>H2S ②原子半径:Na>Mg>O ③酸性:H3PO4>H2SO4>HClO4 ④结合质子能力:OH->CH3COO->Cl-
A.①③ B.②④ C.①④ D.②③
解析:①中热稳定性应与元素非金属性对应,应为HF>H2O>H2S;②同周期元素的半径从左至右逐渐减小,Na>Mg,O在Na和Mg的上一周期,半径最小;③酸性与中心元素的非金属性应该对应,错误;④由OH-+CH3COOH可反应,CH3COO-+HCl可反应即可知正确。
答案:B
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com