
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
27°¢(12∑÷)A°¢B°¢C°¢Dæ˘Œ™«‚ªØŒÔ£¨∆‰∑÷◊”÷–À˘∫¨‘≠◊” ˝“¿¥ŒŒ™2°¢3°¢4°¢4°£A°¢Cµƒ∑÷◊”÷–‘≠◊”∏ˆ ˝±»æ˘Œ™1£∫1£¨«“µÁ◊”◊Ð ˝æ˘Œ™18£ªB”ÎCµƒ‘™Àÿ÷÷¿ýœýÕ¨£ªB°¢D∑÷◊”æ˘∫¨10∏ˆµÁ◊”£¨B”ÎD∑¥”¶µ√µΩ“ª÷÷“ª‘™»ıºÓ°£
«Îªÿ¥£∫
(1)A∑÷◊”µƒµÁ◊” Ω «°°°°°°°°°°°°°°°°°°°°°°°°°° °£
(2) µ—È “÷∆±∏DµƒªØ—ß∑Ω≥Ã Ω «°°°°°°°°°°°°°°°°°°°°°°°°°°°° £ªºÏ—ÈD «∑Ò ’ºØ¬˙µƒ∑Ω∑® «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
(3) µ—È “¿˚”√œ°¡ÚÀ·”Îπ˝—ıªØ±µ∑¢…˙∏¥∑÷Ω‚∑¥”¶¿¥÷∆±∏C£¨∏√∑¥”¶µƒªØ —ß∑Ω≥Ã Ω «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
—ß∑Ω≥Ã Ω «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
 (4)𧓵…œ¿˚”√µÁΩ‚KHSO4»Ð“∫À˘µ√µƒ≤˙ŒÔ”ÎÀÆ∑¥”¶÷∆±∏C°£µÁΩ‚KHSO4»Ð“∫ ±£¨—Ùº´∑¥”¶ Ω «2HSO
(4)𧓵…œ¿˚”√µÁΩ‚KHSO4»Ð“∫À˘µ√µƒ≤˙ŒÔ”ÎÀÆ∑¥”¶÷∆±∏C°£µÁΩ‚KHSO4»Ð“∫ ±£¨—Ùº´∑¥”¶ Ω «2HSO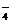 -2e-°°°°°°
S2O
-2e-°°°°°°
S2O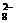 +2H+£¨“ıº´∑¥”¶ Ω «°°°°°°°°°°°°°°°°°°°°°°°°°°°° £ª“—÷™1mol S2O
+2H+£¨“ıº´∑¥”¶ Ω «°°°°°°°°°°°°°°°°°°°°°°°°°°°° £ª“—÷™1mol S2O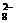 ”ÎÀÆ∑¥”¶µ√µΩC ±◊™“∆¡À2mole-£¨‘Ú∏√∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
”ÎÀÆ∑¥”¶µ√µΩC ±◊™“∆¡À2mole-£¨‘Ú∏√∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
13°¢∏«Àπ∂®¬…»œŒ™ƒÐ¡ø◊Ð « ÿ∫„µƒ£∫ªØ—ß∑¥”¶π˝≥Óª≤ΩÕÍ≥…ªÚ∑÷≤ΩÕÍ≥…£¨’˚∏ˆπ˝≥õƒ»»–ß”¶ «œýÕ¨µƒ°£
 “—÷™£∫¢ŸH2O(g)°°°°°° H2O(1)£ª°˜H= - Q1kJ/mol£ª
“—÷™£∫¢ŸH2O(g)°°°°°° H2O(1)£ª°˜H= - Q1kJ/mol£ª
 ¢⁄C2H5OH(g)°°°°°° C2H5OH(1)£ª°˜H= - Q2kJ/mol£ª
¢⁄C2H5OH(g)°°°°°° C2H5OH(1)£ª°˜H= - Q2kJ/mol£ª
 ¢€C2H5OH(g)+3O2(g)°°°°°° 2CO2(g)+3H2O(g)£ª°˜H= - Q3kJ/mol£ª
¢€C2H5OH(g)+3O2(g)°°°°°° 2CO2(g)+3H2O(g)£ª°˜H= - Q3kJ/mol£ª
œ¬¡–≈–∂œ’˝»∑µƒ «(°° )
A°¢æ∆æ´µƒ»º…’»»Œ™Q3kJ
B°¢»Ù π2 3g“∫ÃÂæ∆æ´ÕÍ»´»º…’£¨◊Ó∫Ûª÷∏¥µΩ “Œ¬£¨ Õ∑≈≥ˆµƒ»»¡øŒ™(1.5Q1-0.5Q2+0.5Q3)kJ
3g“∫ÃÂæ∆æ´ÕÍ»´»º…’£¨◊Ó∫Ûª÷∏¥µΩ “Œ¬£¨ Õ∑≈≥ˆµƒ»»¡øŒ™(1.5Q1-0.5Q2+0.5Q3)kJ
C°¢H2O(g)°˙H2O(1) Õ∑≈≥ˆ¡À»»¡ø£¨À˘“‘∏√π˝≥ÃŒ™ªØ—ß±‰ªØ
D°¢¥”∑¥”¶¢€ø…÷™1molC2H5OH(g)µƒƒÐ¡ø∏þ”⁄2CO2(g)∫Õ3H2O(g)µƒ◊ЃСø
12°¢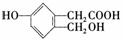 ƒ≥”–ª˙ŒÔ°°°°°°°°°°°°°°°°°°°°
£¨1mol∏√”–ª˙ŒÔ∑÷±”ÎNa°¢NaOH»Ð“∫°¢NaHCO3
ƒ≥”–ª˙ŒÔ°°°°°°°°°°°°°°°°°°°°
£¨1mol∏√”–ª˙ŒÔ∑÷±”ÎNa°¢NaOH»Ð“∫°¢NaHCO3
»Ð“∫∑¥”¶ ±◊Ó∂ýœ˚∫ƒNa°¢NaOH°¢NaHCO3µƒŒÔ÷ µƒ¡ø÷Ʊ»Œ™(°° )
A°¢3£∫2£∫1 °°°°°°°° B°¢3£∫1£∫2°°°°°°°°°° C°¢3£∫2£∫2°°°°°°°°°° D°¢1£∫2£∫3
11°¢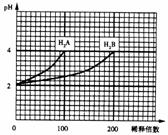 ≥£Œ¬œ¬£¨»°pH=2µƒ¡Ω÷÷∂˛‘™À·H2A”ÎH2B∏˜1ml£¨∑÷±º”ÀÆœ° Õ£¨≤‚µ√PH±‰ªØ”κ”ÀÆœ° Õ±∂ ˝”–»ÁÕºÀ˘ 汉ªØ£¨‘Úœ¬¡–”–πÿ– ˆ’˝»∑µƒ «(°° )
≥£Œ¬œ¬£¨»°pH=2µƒ¡Ω÷÷∂˛‘™À·H2A”ÎH2B∏˜1ml£¨∑÷±º”ÀÆœ° Õ£¨≤‚µ√PH±‰ªØ”κ”ÀÆœ° Õ±∂ ˝”–»ÁÕºÀ˘ 汉ªØ£¨‘Úœ¬¡–”–πÿ– ˆ’˝»∑µƒ «(°° )

 A°¢H2AµƒµÁ¿Î∑Ω≥Ã ΩŒ™H2A°°°°°° H++HA-£¨HA-°°°°°°
H++A2-
A°¢H2AµƒµÁ¿Î∑Ω≥Ã ΩŒ™H2A°°°°°° H++HA-£¨HA-°°°°°°
H++A2-
B°¢PH=4µƒNaHAÀƻГ∫÷–¿Î◊”≈®∂»¥Û–°Œ™
c(Na+)>c(HA-)>c(A2-)>c(H2A)>c(OH-)
C°¢∫¨NaHA°¢NaHBµƒªÏ∫œ»Ð“∫÷–£¨¿Î◊”≈®∂»¥Û–°Œ™
c(Na+)=c(A2-)+c(HB-)+c(H2B)+c(B2-)
D°¢Na2BµƒÀƻГ∫÷–£¨¿Î◊”≈®∂»¥Û–°Œ™c(Na+)>c(B2-)>c(OH-)>c(H+)
10°¢”√”⁄µÁ∂Ø∆˚≥µµƒ¬¡-ø’∆¯»º¡œµÁ≥ÿ£¨Õ®≥£“‘NaCl»Ð“∫ªÚNaOH»Ð“∫Œ™µÁΩ‚“∫£¨¬¡∫œΩŒ™∏∫º´£¨ø’∆¯µÁº´Œ™’˝º´°£œ¬¡–Àµ∑®’˝»∑µƒ «(°° )
 A°¢∑÷±“‘NaCl»Ð“∫∫ÕNaOH»Ð“∫Œ™µÁΩ‚÷ ±£¨∏∫º´∑¥”¶æ˘Œ™£∫Al+3OH--3e- °°°°Al(OH)3°˝
A°¢∑÷±“‘NaCl»Ð“∫∫ÕNaOH»Ð“∫Œ™µÁΩ‚÷ ±£¨∏∫º´∑¥”¶æ˘Œ™£∫Al+3OH--3e- °°°°Al(OH)3°˝
B°¢∑÷±“‘NaCl»Ð“∫∫ÕNaOH»Ð“∫Œ™µÁΩ‚÷ ±£¨’˝º´∑¥”¶≤ªÕ¨
C°¢“‘NaOH»Ð“∫Œ™µÁΩ‚“∫ ±£¨µÁ≥ÿ‘⁄π§◊˜π˝≥Ã÷–µÁΩ‚“∫µƒpHΩµµÕ
D°¢µÁ≥ÿπ§◊˜ ±£¨µÁ◊”Õ®π˝Õ‚µÁ¬∑¥”’˝º´¡˜œÚ∏∫º´
9°¢‘⁄∫„Œ¬°¢∫„—πœ¬£¨1molA∫ÕnmolB‘⁄“ª∏ˆ»ðª˝ø…±‰µƒ»ð∆˜÷–∑¢…˙»Áœ¬∑¥”¶£∫
 A(g)+2B(g)°°°°°° 2C(g)£¨“ª∂Œ ±º‰∫Û¥ÔµΩ∆Ω∫‚£¨…˙≥…amolC°£‘Úœ¬¡–Àµ∑®÷–’˝»∑µƒ «(°° )
A(g)+2B(g)°°°°°° 2C(g)£¨“ª∂Œ ±º‰∫Û¥ÔµΩ∆Ω∫‚£¨…˙≥…amolC°£‘Úœ¬¡–Àµ∑®÷–’˝»∑µƒ «(°° )
A°¢ŒÔ÷ A°¢Bµƒ◊™ªØ¬ ÷Ʊ»Œ™1£∫2
B°¢∆ º ±øÃ∫Õ¥ÔµΩ∆Ω∫‚∫Û»ð∆˜÷–ªÏ∫œ∆¯ÃÂ√Ð∂»œýµ»
C°¢µ±Aµƒ’˝∑¥”¶ÀŸ¬ ”ÎCµƒƒÊ∑¥”¶ÀŸ¬ ÷Ʊ»Œ™2 ±£¨ø…∂œ∂®∑¥”¶¥ÔµΩ∆Ω∫‚◊¥Ã¨
D°¢»Ù∆ º ±∑≈»Î3molA∫Õ3nmolB£¨‘Ú¥ÔµΩ∆Ω∫‚ ±…˙≥…3amolC
8°¢œ¬¡–∏˜◊È¿Î◊”‘⁄Ãÿ∂®µƒ»Ð“∫÷–£¨“ª∂®ƒÐ¥Û¡øπ≤¥Êµƒ «(°° )
|
—°œÓ |
Ãÿ∂®»Ð“∫ |
¿Î◊”◊È |
|
A |
ŒÞ…´»Ð“∫£¨»ÙœÚ∆‰÷–º”»Î◊„¡ø±•∫Õ¬»ÀÆ£¨»Ð“∫≥ ≥»ª∆…´£¨ºÃ–¯µŒº”¬»ªØ±µ»Ð“∫£¨≤˙…˙∞◊…´≥¡µÌ£ª»ÙœÚ‘≠»Ð“∫÷–º”»Î¬¡∑€£¨”–∆¯≈ð≤˙…˙ |
K+°¢Na+°¢H+°¢Br-°¢SO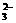 °¢NO °¢NO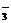 |
|
B |
‘⁄ƒ≥»Ð“∫÷–µŒº”º◊ª˘≥»£¨»Ð“∫±‰ª∆…´ |
Na+°¢Mg2+°¢Cu2+°¢MnO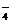 °¢Br-°¢SO °¢Br-°¢SO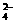 |
|
C |
¡ÚÀ·«‚ƒ∆”Ϋ‚—ıªØ±µµƒªÏ∫œ»Ð“∫ |
Na+°¢K+°¢NO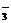 °¢Cl-°¢I- °¢Cl-°¢I- |
|
D |
25°ÊÀƵÁ¿ÎµƒH+≈®∂»Œ™1°¡10-10mol/Lµƒ»Ð“∫ |
Al3+°¢NH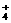 °¢Fe2+°¢SO °¢Fe2+°¢SO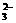 °¢S2- °¢S2- |
7°¢”√NA±Ì æ∞¢∑¸º”µ¬¬Þ≥£ ˝µƒ÷µ°£œ¬¡–– ˆ’˝»∑µƒ «(°° )
A°¢∫¨NA∏ˆNa+µƒNa2O»ÐΩ‚‘⁄1LÀÆ÷–£¨Na+µƒŒÔ÷ µƒ¡ø≈®∂»Œ™1mol/L
B°¢0.15molFe3O4»Ð”⁄◊„¡øœıÀ·»Ð“∫£¨◊™“∆µƒµÁ◊” ˝ Œ™0.15NA
Ϊ0.15NA
C°¢1L0.1mol/Lµƒ¥◊À·»Ð“∫÷–À˘∫¨µƒ¿Î◊”∫Õ∑÷◊”◊Ð ˝Œ™0.1NA
D°¢1.2gNaHSO4æßÃÂ÷–—Ù¿Î◊”∫Õ“ı¿Î◊”µƒ◊Ð ˝Œ™0.03NA
6°¢◊‘±£∂® –±ª ¿ΩÁ◊‘»ªª˘Ωª·—°∂®Œ™°∞÷–π˙µÕú≥« –∑¢’πœÓƒø°±µƒ ◊≈˙ ‘µ„≥« –÷Æ∫Û£¨°∞µÕú°±“—æ≠◊þΩ¯∞Ÿ–’…˙ªÓ°¢≥« –Ω®…Ë“‘º∞æ≠º√∑¢’πµ»∏˜∏ˆ¡Ï”Ú£¨œ¬¡–”–πÿÀµ∑®≤ª’˝»∑µƒ «(°°
A°¢Ã´—كа¢µÿ»»ƒÐ°¢∫ÀƒÐµ»æ˘ Ù”⁄–¬ƒÐ‘¥
 B°¢°∞µÕú°± «÷∏≤…”√∫¨Ãº¡øµÕµƒÃ˛¿ýªØ∫œŒÔ◊˜»º¡œ
B°¢°∞µÕú°± «÷∏≤…”√∫¨Ãº¡øµÕµƒÃ˛¿ýªØ∫œŒÔ◊˜»º¡œ
C°¢Õº÷–º◊ÕÈæ≠“ª¬»º◊ÕÈ◊™ªØ≥…µÕúœ©Ã˛µƒÕææ∂ÃÂœ÷¡À°∞Ω⁄ƒÐºı≈≈°±ÀºœÎ
D°¢ºı…ŸªØ ؃Б¥µƒ π”√ƒÐºı…ŸCO2µƒ≈≈∑≈¡ø
29.(15∑÷)‘⁄𧓵…œœ©Ã˛ø…“‘∫œ≥…∂ý÷÷”–ª˙≤ƒ¡œ°£
(1)ƒ≥Õ¨—߅˺∆¡À”…““œ©∫œ≥…Yµƒ3Ãı¬∑œþ(I°¢II°¢III)»Áœ¬ÕºÀ˘ æ°£
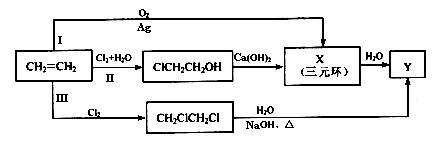
¢Ÿ 3Ãı∫œ≥…¬∑œþ÷–£¨ƒ„»œŒ™∑˚∫œ°∞‘≠◊”æ≠º√°±w.w.^w.k.&s.5*
“™«Ûµƒ∫œ≥…¬∑œþ «(ÃÓ–Ú∫≈°∞I°±°¢ °∞II°±ªÚ°∞III°±)°°°°°° °£
¢⁄ XµƒΩ·ππºÚ Ω «°°°°°°°°°°°°°°°° °£
(2)“—÷™QŒ™““œ©µƒÕ¨œµŒÔ£¨“‘Q∫ÕXŒ™‘≠¡œ∫œ≥…Mµƒ∑Ω∑®»Áœ¬£∫
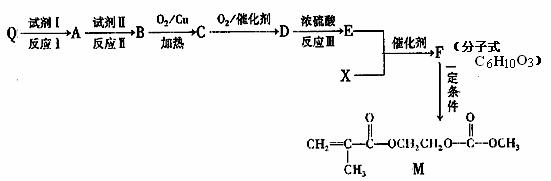
«Îªÿ¥œ¬¡–Œ £∫
¢ŸQµƒ√˚≥∆ «°°°°°°°°°°°°°°°°°°°°
¢⁄E÷–∫¨”–πŸƒÐÕ≈µƒ√˚≥∆ «°°°°°°°°°°°°°° °°£¨FµƒΩ·ππºÚ Ω «°°°°°°°°°°°°°°°° .
¢€–¥≥ˆM”Î◊„¡ø«‚—ıªØƒ∆»Ð“∫∑¥”¶µƒªØ—ß∑Ω≥Ã Ω°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
¢Ð“—÷™£∫
 w.w.^w.k.&s.5*
w.w.^w.k.&s.5*
GµƒÕ¨∑÷“ÏππÔ–∂ý÷÷£¨–¥≥ˆ∑˚∫œœ¬¡–Ãıº˛µƒGµƒÀ˘”–Õ¨∑÷“Ïππð°°°°°°°
°°°°°°°°°°°°°°°°
a£Æ”΃∆∑¥”¶∑≈≥ˆ«‚∆¯°°°° b£Æ‘⁄À·–‘Ãıº˛œ¬ÀÆΩ‚Œ™N∫Õ““¥º°° c. N÷–∫¨”–÷ß¡¥
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com