
题目列表(包括答案和解析)
2.对于醋酸溶液的下列说法中,不正确的是( )
A.醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-)
B.醋酸溶液中加入少量醋酸钠晶体,醋酸电离程度减小
C.0.1 mol·-1L的醋酸溶液中加水稀释,溶液中c(OH-)减小
D.常温下,pH=3的醋酸溶液与pH=11的烧碱溶液等体积混合后,溶液中c(H+)>c(OH-)
1.物质的量相同的下列溶液中,含微粒种类最多的是( )
A.CaCl2 B.CH3COONa
C.NH3 D.K2S
12.(2009年梁丰质检)已知Ksp(AgCl)=c(Ag+)·c(Cl-)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12,某同学通过实验验证醋酸银(CH3COOAg)的Ksp,实验中用了如下反应:2Ag+(aq)+Cu(s)=2Ag(s)+Cu2+(aq),该学生将已知质量的铜片加入到CH3COOAg饱和溶液中,待充分反应后,将铜片冲洗干净、重新称量。
(1)CH3COOAg的Ksp=2.0×10-3,没反应前铜片的质量为23.4 g,将铜片放在100 mL的CH3COOAg饱和溶液中,此饱和溶液中没有CH3COOAg固体,通过计算说明充分反应后铜片中铜的质量为何值时,CH3COOAg的Ksp得到证实。
(2)为什么做此实验时CH3COOAg饱和溶液中必须没有CH3COOAg固体?
11.(2009年海南模拟)如下图所示,横坐标为溶液的pH值,纵坐标为Zn2+离子或
Zn(OH) 42-,离子物质的量浓度的对数,回答下列问题。
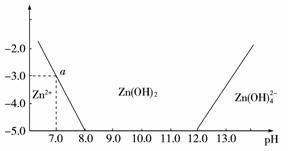
(1)往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为:____________ 。
(2)从图中数据计算可得Zn(OH)2的溶度积(Ksp)=-____________________________________ 。
(3)某废液中含Zn2+离子,为提取Zn2+离子可以控制溶液中pH值的范围是____________ 。
(4)往100 L 1.00 mol·-1L ZnCl2溶液中加入NaOH固体至pH=6,需NaOH____________ mol。
(5)已知:往ZnCl2溶液中加入硝酸铅或醋酸铅溶液可以制得PbCl2白色晶体;25 ℃时,PbCl2固体在盐酸中的溶解度如下:
|
c(HCl)/(mol·-1L) |
0.50 |
1.00 |
2.04 |
2.90 |
4.02 |
5.16 |
5.78 |
|
c(PbCl2)/(mol·-1L)×10-3 |
5.10 |
4.91 |
5.21 |
5.90 |
7.48 |
10.81 |
14.01 |
根据上表数据判断下列说法正确的是____________(填字母序号)
A.随着盐酸浓度的增大,PbCl2固体的溶解度先变小后又变大
B.PbCl2固体在0.50 mol·-1L盐酸中溶解度小于在纯水中的溶解度
C.PbCl2能与浓盐酸反应生成一种难电离子的阴离子(如配合离子)
D.PbCl2固体可溶于饱和食盐水
10.已知常温下,FeS的Ksp=6.25×10-18 mol2·L-2,ZnS的Ksp=1.2×10-23 mol2·L-2,H2S的饱和溶液中[H+]与[S2-]之间存在如下关系:[H+]2·[S2-]=1.0×10-22 mol3·L-3。试回答下列有关问题:
(1)向ZnS的饱和溶液中:①加入少量固体Na2S,则溶液中[S2-]____________(填“变大”、“变小”或“不变”,下同);②加入ZnS固体,则溶液中[S2-]____________;③加入FeS固体,则溶液中[Zn2+]____________。
(2)在常温下,将适量的FeS投入到氢硫酸饱和溶液中,欲使溶液中[Fe2+]达到1 mol/L,应调节溶液的pH=__________(已知:lg2=0.3)。
9.氧化还原滴定法是以氧化还原反应为基础的滴定分析方法,其中一种叫高锰酸钾法。由于在微酸、 中性和弱碱性溶液中,MnO4-被还原为棕色不溶物MnO2,使溶液混浊而妨碍滴定终点的观察,因此高锰酸钾法通常在较强的酸性溶液中进行。
(1)酸化高锰酸钾时,能不能使用盐酸____________(答“能”或“不能”),理由是(回答“不能”,此问作答,回“能”,此空不填,下同)____________;能否使用HNO3____________(答“能”或“不能”),理由是:____________ 。
(2)KMnO4标准溶液常用还原物质来标定。常用的还原物质为Na2C2O4等。其标定反应向下:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O
滴定开始时,是否需要滴加指示剂?____________(填“是”或“否”),理由是____________ 。
(3)用KMnO4标准溶液在酸性溶液中可测定H2O2样品中H2O2的含量,反应如下:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O。
①温度不变,反应开始较慢,随着反应的进行,反应速度明显加快,可能的原因是____________ 。
②该反应中H2O2为____________剂。
8.(思维拓展题)已知Ksp(AgCl)=1.8×10-10 mol2·L-2,Ksp(AgI)=1.0×10-16 mol2·L-2。下列关于不溶物之间转化的说法中正确的是( )
A.AgCl、AgI两者都不溶于水,因此AgCl与AgI不能相互转化
B.常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于1/1.8×10-11 mol·-1L
C.一定条件下AgCl可以转化为更难溶的AgI
D.只能由Ksp较大的不溶物转化为Ksp较小的不溶物
7.已知25 ℃时,Ka(HF)=3.6×10-4,Ksp(CaF2)=1.46×10-10。现向1 L 0.2 mol·-1L HF溶液中加入1 L 0.2 mol·-1L CaCl2溶液,则下列说法中,正确的是( )
A.25 ℃时,0.1 mol·-1L HF溶液中pH=1
B.Ksp(CaF2)随温度和浓度的变化而变化
C.该体系中有沉淀产生
D.该体系中HF与CaCl2反应产生沉淀
6.(2010年板浦模拟)一定温度下的难溶电解质AmBn在水溶液中达到沉淀溶解平衡时,其平衡常数Ksp=[An+]m[Bm-]n,称为难溶电解质的溶度积。已知下表数据:
|
物质 |
Fe(OH)2 |
Cu(OH)2 |
Fe(OH)3 |
|
Ksp/25 ℃ |
8.0×10-16 |
2.2×10-20 |
4.0×10-38 |
|
完全沉淀时的pH范围 |
≥9.6 |
≥6.4 |
3~4 |
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法,不科学的是( )
A.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
B.该溶液中[SO42-]∶([Cu2+]+[Fe2+]+[Fe3+])>5∶4
C.向该溶液中加入适量氯水,并调节pH到3~4过滤,可获得纯净的CuSO4溶液
D.在pH=5的溶液中Fe3+不能大量存在
5.(2009年聊城模拟)已知如下物质的溶度积常数FeS:Ksp=6.3×10-18 mol2·L-2;CuS:Ksp=1.3×10-36mol2·L-2。下列说法正确的是( )
A.同温度下,CuS的溶解度大于FeS的溶解度
B.同温度下,向饱和FeS溶液中加入少量Na2S固体后,Ksp(FeS)变小
C.向含有等物质的量的FeCl2和CuCl2的混合溶液中逐滴加入Na2S溶液,最先出现的沉淀是FeS
D.除去工业废水中的Cu2+,可选用FeS做沉淀剂
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com