
题目列表(包括答案和解析)
6. 下列涉及有机物的说法正确的是
A.互为同分异构体的物质一定不是同系物
B.甲酸的性质与乙酸类似,都不能被酸性高锰酸钾溶液氧化
C.乙醇转化为乙醛的反应有碳氧双键生成,属于消去反应
D.纤维素、蔗糖、葡萄糖和淀粉酶在一定条件下都可发生水解反应
28. (1)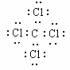
A:HO- -CH2CH=CH2 C:NaO-
-CH2CH=CH2 C:NaO- -CH2CHO E:HO-
-CH2CHO E:HO- -CH=CH2(或相应的间位、邻位)
-CH=CH2(或相应的间位、邻位)
(2)HO- -CHO
-CHO 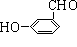 ;
;  HCOO-
HCOO- ;
;  -COOH
-COOH
29(1).(6分)(1)NO
(2)CH4 (3)NH3·H2O (4)CO
(5)BaSO4或Ca(HCO3)2 (6)氨水
(2).(每空1分,共6分)
|
步骤 |
操作过程 |
实验现象 |
结论 |
|
① |
称取等质量的CuO、CuS、Cu2S粉末各一份, |
/ |
/ |
|
② |
把三分样品分别在空气中灼烧, |
有两种固体产生刺激性气味的气体,另种无气味。 |
有气味的是CuS与Cu2S粉末,无刺激性气体产生的CuO粉末。 |
|
③ |
称量灼烧后不再产生刺激性气体的冷却残留物, |
一种质量几乎不变,一种质量减轻。 |
质量几乎不变的原粉末为Cu2S。质量减轻的原粉末是CuS。 |
27、(7分)(1) Si3N4 (1分) SiCl4 (1分) (2) Si3N4+3O2=3SiO2+2N2 (2分)
(3) +4 (1分) -3 (1分)原子晶体(1分)
26.(共12分)
(1)Ⅰ:B Ⅱ:A Ⅲ:E (各1分,共3分)
(2)检查装置的气密性 (1分)
(3)保持分液漏斗内压强与烧瓶内压强相等 (1分)
(4)先加热催化剂,然后缓慢滴加浓硫酸 (1分)
(5)温度过高不利于SO3的生成,且影响催化剂的活性。 (2分) 降低 (1分)
(6) 70.5% (3分)
6.B 7.D 8.C 9.A 10.B 11.C 12.A 13.C
29.(1)科学家在研究化学物质时,常常对物质进行分类,以便对同类物质的组成和性能进行探入的研究。下列各组物质中有一种物质与其它物质不属于同一类,请将其挑出来。
|
物质组 |
不属于同类的物质 |
|
(1)Mg、O2、I2、NO |
|
|
(2)NaOH、Na2CO3、CH4、CaO |
|
|
(3)HClO、H2SO4、NH3H2O、H2SiO3 |
|
|
(4)CO、SO2、CO2、SO3 |
|
|
(5)Ca(HCO3)2、Na2CO3、AgNO3、BaSO4 |
|
|
(6)水、液氯、氨水、水银 |
|
*(2)现有CuO、CuS、Cu2S三种黑色粉末,请设计一个不用化学药品就可区分它们的实验方案。(请用文字叙述)
|
步骤 |
操作过程 |
实验现象 |
结论 |
|
① |
称取等质量的CuO、CuS、Cu2S粉末各一份, |
/ |
/ |
|
② |
|
|
|
|
③ |
|
|
|
化学知识点考察检测(3)
28. 在一定条件下,烯烃可发生臭氧化还原水解反应,生成羰基化合物,该反应可表示为:

已知:
① 化合物A,其分子式为C9H10O,它既能使溴的四氯化碳溶液褪色,又能与FeCl3溶液发生显色反应,且能与金属钠或氢氧化钠溶液反应生成B;
② B发生臭氧化还原水解反应生成C,C能发生银镜反应;
③ C催化加氢生成D,D在浓硫酸存在下加热生成E;
④ E既能使溴的四氯化碳溶液褪色,又能与FeCl3溶液发生显色反应,且能与氢氧化钠溶液反应生成F;
⑤ F发生臭氧化还原水解反应生成G,G能发生银镜反应,遇酸转化为H(C7H6O2)。
请根据上述信息,完成下列填空:
(1)写出下列化合物的结构简式(如有多组化合物符合题意,只要写出其中的一组)
A_________ _______,C______ _________,E____________________。
(2)写出分子式为C7H6O2的含有苯环的所有同分异构体的结构简式_____________。
27. 由新型无机非金属材料制成的无水冷发动机,热效率高、寿命长。 这类材料中研究较多的是化合物G。
(1)化合物G 的相对分子质量为140,G 中含硅元素,其质量分数为60%,另有元素Y。
G 可以由化合物E(含两种元素)与NH3反应而生成,同时产生HCl 气体。
请推断:G 和E的化学式分别为______________、______________。
(2)粉末状G 能够与氧气反应,所得产物中有一种是空气中的主要成分,另一种是工业
上生产玻璃的主要原料。请写出化合物G 与氧气反应的化学方程式
(3)常压下在G 中添加氧化铝,经高温烧结可制成一种高强度、超硬废、耐磨损、抗腐蚀
的陶瓷材料,它的商品名叫“赛伦”,化学通式可表示为Si6-XAlXOXY8-X。在接近1700℃时x的极限值约为4.0,在1400℃时 x为2.0,以保持整个化合物呈电中性。推测:
赛伦中以下元素的化合价:Si_______Y______,塞伦的晶体类型__________
26.
用下图装置进行SO2转化为SO3的转化率测定实验:2SO2+O2  2SO3 △H=-196.6kJ/mol
2SO3 △H=-196.6kJ/mol
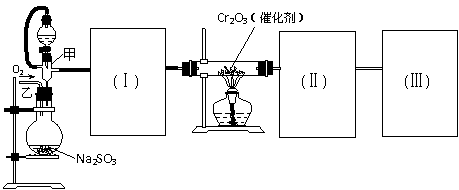
(1)要顺利进行实验,上图Ⅰ、Ⅱ、Ⅲ处各应连接1个合适的装置,请从下列A~E中选择适宜的装置,将其序号填入空格内。

Ⅰ 、Ⅱ 、Ⅲ 。
(2)实验前,必须进行的操作是(填操作名称,不必写具体过程)
(3)实验时,浓硫酸能顺利滴入烧瓶中,甲装置所起作用的原理是: 。
(4)从乙处均匀通入O2,为使SO2有较高的转化率,实验时滴入浓硫酸与加热催化剂的先后顺序是 。
*(5)实验中当Cr2O3表面红热时,应将酒精灯移开一会儿再加热,以防温度过高,这样做的原因是 若用大火加热有Cr2O3处的反应管时,SO2的转化率会 (填升高、降低或不变)
(6)实验时若用25.2g的Na2SO3,加入的浓硫酸是足量的,反应结束时继续通入O2一段时间,称得Ⅱ处装置的质量增加11.3g,则本实验中SO2的转化率为 。(保留3位有效数字)
13、右图是恒温下某化学反应的反应速率随反应时间变化的示意图。下列叙述与示意图

不相符合的是
A.反应达平衡时,正反应速率和逆反应速率相等
B.该反应达到平衡态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡态Ⅱ
C.该反应达到平衡态Ⅰ后,减小反应物浓度,
平衡发生移动,达到平衡态Ⅱ
D.同一种反应物在平衡态Ⅰ和平衡态Ⅱ时浓度不相等
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com