
题目列表(包括答案和解析)
12. 下表是元素周期表的一部分,回答下列有关问题:
|
族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
2 |
|
|
|
|
① |
|
② |
|
|
3 |
③ |
④ |
⑤ |
⑥ |
|
⑦ |
⑧ |
|
|
4 |
⑨ |
|
|
|
|
|
⑩ |
|
(1)写出下列元素符号:
① ,⑥ ,⑦ ,⑧ 。
(2)在这些元素中,最活泼的金属元素是 ,最活泼的非金属元素是 。
(3)在这些元素中的最高价氧化物对应的水化物中,酸性最强的是 ,碱性最强的是 ,呈两性的氢氧化物是 ,写出三者之间相互反应的离子方程式: ; ; 。
(4)在这些元素中,原子半径最小的是 ,原子半径最大的是 。
(5)在③与④中,化学性质较活泼的是 ,怎样用化学实验证明?
。
在⑧与⑩中,化学性质活泼的是 ,怎样用化学实验证明?
。
11. 有三种短周期元素,最外层电子数之和为17,质子数之和为31。如果这三种元素中有一种是氩元素,则关于另外两种元素的说法不正确的是( )
A. 如果一种元素是金属元素,则另一种元素可能是稀有气体元素
B. 如果一种元素的单质通常情况下是气体,则另一种元素的单质通常情况下是固体
C. 如果一种元素的气态氢化物能使湿润的红色石蕊试纸变蓝,则另一种元素的气态氢化物则使湿润的蓝色石蕊试纸变红
D. 如果一种元素的最高正价是+3,则另一种元素的单质有两种常见的同素异形体
10. 短周期元素A、B、C的原子序数依次递增。已知A、C同主族,而且三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半。下列叙述正确的是( )
A. 原子半径:A<B<C
B. 沸点:A的氢化物低于C的氢化物
C. B的硫酸盐溶液pH<7
D. B元素单质可溶于酸但不溶于碱
9. 元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构。下列推测不正确的是( )
A. 同周期元素中X的金属性最强
B. 原子半径X>Y,离子半径X+>Z2-
C. 同族元素中Z的氢化物稳定性最高
D. 同周期元素中Y的最高价含氧酸的酸性最强
8. (2007年高考广东卷·化学)短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13。X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的3倍。下列说法正确的是( )
A. X的氢化物溶于水显酸性
B. Y的氧化物是离子化合物
C. Z的氢化物的水溶液在空气中存放不易变质
D. X和Z的最高价氧化物对应的水化物都是弱酸
7. (2007年高考广东卷·理基)下列关于元素周期表和元素周期律的说法错误的是( )
A. Li、Na、K元素的原子核外电子层数随着核电荷数的增加而增多
B. 第二周期元素从Li到F,非金属性逐渐增强
C. 因为Na比K容易失去电子,所以Na比K的还原性强
D. O与S为同主族元素,且O比S的非金属性强
6. 短周期元素X、Y、Z在元素周期表中的位置关系如右图所示,则下列关于X、Y、Z的描述中,正确的是( )
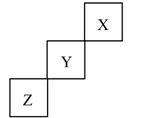
A. Z一定是活泼的金属元素
B. X是非金属性最强的元素
C. 1 mol Y单质与足量水反应时,发生转移的电子数为2 NA( NA为阿伏加德罗常数)
D. Z元素的最高价氧化物对应的水化物是H3ZO4
5. (2007年高考山东卷·理综)下列关于元素的叙述正确的是( )
A. 金属元素与非金属元素能形成共价化合物
B. 只有在原子中,质子数才与核外电子数相等
C. 目前使用的元素周期表中,最长的周期含有36种元素
D. 非金属元素形成的共价化合物中,原子的最外层电子数只能为2或8
4. 甲、乙两元素原子的L层电子数都是其他层电子总数的2倍。下列推断正确的是( )
A. 甲与乙处于同一周期
B. 甲与乙处于同一主族
C. 甲单质不可能从乙的化合物中置换出乙单质
D. 甲与乙的原子序数之和为偶数
3. 第7周期为不完全周期,若将来的发现把这一周期元素全部排满。则下列有关第7周期元素的推论可能错误的是( )
A. 第7周期排满时有32种元素
B. 第7周期排满时最后一种单质可与一些物质发生化学反应
C. 第7周期第ⅦA族元素原子序数117,是一种金属元素
D. 第7周期第ⅢA族元素的氢氧化物与Al(OH)3都具有两性
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com