
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
6. ÓĆŅ»¼ŪĄė×Ó×é³ÉĖÄÖÖŃĪ£¬AC”¢BD”¢AD”¢BCµÄ1mol”¤L-1 ČÜŅŗ£¬ŌŚŹŅĪĀĻĀĒ°Į½ÖÖČÜŅŗµÄpH£½7£¬µŚČżÖÖČÜŅŗµÄpH >7£¬×īŗóŅ»ÖÖČÜŅŗµÄpH< 7£¬Ōņ(B)
|
”” |
A |
B |
C |
D |
|
¼īŠŌ |
AOH>BOH |
AOH<BOH |
AOH>BOH |
AOH<BOH |
|
ĖįŠŌ |
HC>HD |
HC>HD |
HC<HD |
HC<HD |
5. ÅØ¶Č¾łĪŖ0.1 mol / LµÄ¢ŁNaHCO3”¢¢ŚNa2CO3”¢¢ŪNaCl”¢¢ÜNaHSO4ĖÄÖÖČÜŅŗ£¬°“pHÖµÓÉŠ”µ½“óÅÅĮŠµÄĖ³ŠņŹĒ”” (”” ) ””A. ¢Ł¢Ś¢Ū¢Ü”” B.¢Ü¢Ū¢Ł¢Ś””””””C.¢Ū¢Ü¢Ł¢Ś”””” D.¢Ś¢Ł¢Ü¢Ū
4. ĪļÖŹµÄĮæÅضČĻąĶ¬µÄČżÖÖŃĪNaX”¢NaYŗĶNaZµÄČÜŅŗ£¬ĘäpHÖµŅĄ“ĪĪŖ8”¢9”¢10£¬ŌņHX”¢HY”¢HZµÄĖįŠŌÓÉĒæµ½ČõµÄĖ³ŠņŹĒ(”””” )
A. HX”¢HZ”¢HY”” B. HZ”¢HY”¢HX”” C. HX”¢HY”¢HZ”””” D. HY”¢HZ”¢HX
3. Ņ»ŌŖĖįHAČÜŅŗÖŠ£¬¼ÓČėŅ»¶ØĮæĒæ¼īMOHČÜŅŗŗó£¬Ē”ŗĆĶźČ«·“Ó¦£¬·“Ó¦ŗóµÄČÜŅŗÖŠ£¬ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ(”” ) ””A£®c(A£) ”Ż c(NH4+)”””””””” B. c(A£) ”Ü c(M+)”” ””C.””ČōMA²»Ė®½ā,Ōņc( OHØD)£¼c(A£)””D.ČōMAĖ®½ā,Ōņc( OHØD)£¾c(A£)
2. µ±Mg(OH)2ŌŚĖ®ÖŠ“ļµ½ČܽāĘ½ŗāŹ±£ŗMg(OH)2  Mg2++2OH£ ŅŖŹ¹Mg(OH)2½ųŅ»²½Čܽā£¬Ó¦ĻņČÜŅŗÖŠ¼ÓÉŁĮæµÄ¹ĢĢåŹĒ””””””
(””
)
””A. NH4Cl”””””” B.
NaOH”””””” C. Na2CO3””””””
D.øɱł
Mg2++2OH£ ŅŖŹ¹Mg(OH)2½ųŅ»²½Čܽā£¬Ó¦ĻņČÜŅŗÖŠ¼ÓÉŁĮæµÄ¹ĢĢåŹĒ””””””
(””
)
””A. NH4Cl”””””” B.
NaOH”””””” C. Na2CO3””””””
D.øɱł
1. ÕōøÉFeCl3Ė®ČÜŅŗŗóŌŁĒæČČ£¬µĆµ½µÄ¹ĢĢåĪļÖŹÖ÷ŅŖŹĒ”””” (”” ) ””A.FeCl3”””” B.FeCl3”¤6H2O””C. Fe(OH)3”””” D. Fe2O3””””””
13.ĒæĖįČõ¼īŃĪÓėĒæ¼īČõĖįŃĪČÜŅŗĻą»ģŗĻ£¬ĘäĻÖĻó²»ÄÜÓĆø“·Ö½ā·“Ó¦¹ęĀɽāŹĶŹ±£¬ŅŖæ¼ĀĒŃĪµÄĖ®½ā”£ČēÅŻÄĆš»šĘ÷µÄŌĄķŹĒAl3++3HCO3-==== Al(OH)3”ż+3CO2”ü£»Ź¹ÓĆĖ®ÄąŹ±¼ÓČėŹŹĮæµÄNH4CæÉ-¼ÓĖŁĖ®ÄąÄż½į£ŗ SiO32- + 2NH4+”” +”” 2H2O==H2SiO3 ”ż + 2NH3”¤ H2O
ŃĪĄąĖ®½āµÄÓ¦ÓĆ×ØĢāѵĮ·
12.ijŠ©»īĘĆ½šŹōÓėĒæĖįČõ¼īŃĪČÜŅŗ·“Ó¦Ź±£¬ŅŖæ¼ĀĒŃĪµÄĖ®½ā”£ČēĆ¾Ģõ²åČėCuSO4ČÜŅŗÖŠÓŠH2·Å³ö£¬ŅņĪŖCu2++2H2O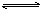 Cu(OH)2+2H+£¬Mg+2H+=== Mg2++H2”ü£»Ķ¬ŃłµĄĄķ£¬ŌŚNH4ClČÜŅŗÖŠĶ¶ČėĆ¾·Ū»įµĆµ½Į½ÖÖĘųĢ壬Ņ²ŹĒÕāøöŌŅņNH4++H2O
Cu(OH)2+2H+£¬Mg+2H+=== Mg2++H2”ü£»Ķ¬ŃłµĄĄķ£¬ŌŚNH4ClČÜŅŗÖŠĶ¶ČėĆ¾·Ū»įµĆµ½Į½ÖÖĘųĢ壬Ņ²ŹĒÕāøöŌŅņNH4++H2O
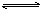 ””NH3”¤H2O+ H+£¬NH3”¤H2O
””NH3”¤H2O+ H+£¬NH3”¤H2O NH3”ü+H2O£¬Mg+2H+=== Mg2++H2”ü”£
NH3”ü+H2O£¬Mg+2H+=== Mg2++H2”ü”£
11.ÅŠ¶ĻÖŠŗĶµĪ¶ØÖÕµć£¬Ń”ÓĆŗĻŹŹµÄĖį¼īÖøŹ¾¼ĮŹ±£¬ŅŖæ¼ĀĒŃĪµÄĖ®½ā”£ČēĒæĖįµĪ¶ØČõ¼īŹ±Ņ»°ćÓĆ¼×»ł³Č£¬ŅņĪŖÉś³ÉµÄŃĪĖ®½ā³ŹĖįŠŌ£¬¼×»ł³ČµÄ±äÉ«·¶Ī§ĪŖ3.1-4.4£¬ĀäŌŚĖįŠŌ·¶Ī§Ö®ÄŚ£¬Ź¹ŹµŃéĪó²īŠ”£»Ķ¬ŃłµĄĄķ£¬Ēæ¼īµĪ¶ØČõĖįŹ±Ņ»°ćÓĆ·ÓĢŖ£¬ŅņĪŖÉś³ÉµÄŃĪĖ®½ā³Ź¼īŠŌ£¬·ÓĢŖµÄ±äÉ«·¶Ī§ĪŖ8-10£¬ĀäŌŚ¼īŠŌ·¶Ī§Ö®ÄŚ
10.½āŹĶijŠ©Éś»īĻÖĻóŹ±Ó¦æ¼ĀĒµ½ŃĪµÄĖ®½ā”£ĄżČēÕØÓĶĢõŹ±ĄūÓĆĮĖĆ÷·ÆÖŠAl3+ÓėŠ”ĖÕ“ņÖŠHCO3-(CO32-)Ė«Ė®½āµÄµĄĄķ£»¼ŅĶ„ÖŠÓĆČȵÄNa2CO3ČÜŅŗĻ“µÓ²Ķ¾ßŠ§¹ūŗĆ£¬ŌŅņŹĒŃĪµÄĖ®½ā¹ż³Ģ¶¼ŹĒĪüČČ¹ż³Ģ£¬¼ÓČČ“Ł½ųCO32-µÄĖ®½ā£¬Ź¹ČÜŅŗÖŠ¼īŠŌŌöĒæ£¬Č„ĪŪÄÜĮ¦¼Ó“ó
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com