
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
26.(1)20%ЎЎЎЎЎЎЎЎЎЎ (2)3.93 mol/LЎЎЎЎЎЎ (3)4.27 mol
24.(1)20ЎЎЎЎЎЎ (2)50ЎЎ 25.(1)0.15 molЎЎЎЎ (2)141.4 g (3)7
23.(1)ТтОӘФЪ10ЎжЎў40ЎжЎў75ЎжКұКЈУа№ММеБҝТАҙОјхЙЩЈ¬ЛщТФЛөГч10ЎжәН40ЎжКұИЬТәТ»¶ЁКЗ ұҘәНөДЎЈ
ЙијУИлөДЛ®ОӘx.
(104-81)ЎГ100ЈҪ(201-132)ЎГxЈ¬ҪвөГxЈҪ300 g
(2)ФЪ75ЎжКұЈ¬»мәПОпЦРПхЛбДЖКЗ·сИ«ІҝИЬҪвБЛ?Йи40ЎжөҪ70ЎжКұЈ¬ФЪ300gЛ®ЦРУЦИЬҪвБЛy g ПхЛбДЖЎЈ
(150-104)ЎГ100ЈҪyЎГ300Ј¬ҪвөГyЈҪ138 gЈҫ(132-72) g
ЛөГчПхЛбДЖФЪ70ЎжЦ®З°ҫНТСИ«ІҝИЬҪвБЛЎЈ
Йи10ЎжКұ300 gЛ®ЦРИЬҪвБЛzЎЎgПхЛбДЖЎЈ
81ЎГ100ЈҪzЎГ300Ј¬ЎЎЎЎ zЈҪ243 g
ҙУ10ЎжөҪ75ЎжУЦИЬҪвөДПхЛбДЖЈә201-72ЈҪ129(g)
»мәПОпЦРЧЬ№Іә¬ПхЛбДЖЈә243+129ЈҪ372(g)ЎЈ
(3)ЙиtЎжКұПхЛбДЖЗЎәГИЬҪвФЪ300 gЛ®ЦРЈ¬ҙЛКұПхЛбДЖөДИЬҪв¶ИОӘS gЎЈ
SЎГ100ЈҪ372ЎГ300Ј¬ЎЎЎЎ SЈҪ124 g
ІйПхЛбДЖИЬҪв¶ИұнҝЙөГОВ¶ИОӘ60ЎжЎЈ№КНкИ«ИЬҪв»мәПОпЦРПхЛбДЖЛщРиЧоөНОВ¶ИОӘ60ЎжЎЈ
22.(1)80%ЎЎЎЎ (2)40%
21.Mg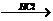 H2Ј¬ЛбЧгБҝКұЎч1ЎЎ ЈҪ
H2Ј¬ЛбЧгБҝКұЎч1ЎЎ ЈҪ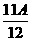 Ј¬ЛбІ»ЧгКұ ҰӨ1ЈҪA-1ЎЈAl
Ј¬ЛбІ»ЧгКұ ҰӨ1ЈҪA-1ЎЈAl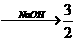 H2Ј¬јоЧгБҝКұҰӨ2ЈҪ
H2Ј¬јоЧгБҝКұҰӨ2ЈҪ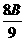 Ј¬јоІ»ЧгКұҰӨ2ЈҪB-3.
Ј¬јоІ»ЧгКұҰӨ2ЈҪB-3.
ўЩЎЎ Лбјоҫщ№эБҝКұЈ¬ТӘК№МмЖҪЖҪәвРиҰӨ1ЈҪҰӨ2Ј¬УР өД№ШПөЈ¬ИЎЦө·¶О§0ЈјAЈј12КЗ¶ФөДЎЈ0ЈјBЈј27КЗІ»¶ФөДЈ¬ТтОӘІъЙъөИБҝH2Кұ әДAlБҝұИMgЙЩЈ¬№КУҰУЙBЈҪ
өД№ШПөЈ¬ИЎЦө·¶О§0ЈјAЈј12КЗ¶ФөДЎЈ0ЈјBЈј27КЗІ»¶ФөДЈ¬ТтОӘІъЙъөИБҝH2Кұ әДAlБҝұИMgЙЩЈ¬№КУҰУЙBЈҪ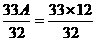 ЈҪ12.3 75Ј¬өГ0ЈјBЈј12.375.ўЪЎЎ ЛбјоҫщІ»ЧгКұЈ¬Іў·ЗAЈҪBЈҫ12Ј¬УҰКЗA-1ЈҪB-3Ј¬јҙAЈҪB-2Ј¬ХвКЗ№Ш
јьЈ¬ИЎЦө·¶О§BЈҫ27Ј¬AЈҫ25¶шОЮЙППЮ(Ц»Ри·ыәПAЈҪB-2)ЎЈўЫЎЎ Лб¶ФMgІ»ЧгЈ¬јо¶ФAlУРУаКұЈ¬УҰОӘA-1ЈҪ
ЈҪ12.3 75Ј¬өГ0ЈјBЈј12.375.ўЪЎЎ ЛбјоҫщІ»ЧгКұЈ¬Іў·ЗAЈҪBЈҫ12Ј¬УҰКЗA-1ЈҪB-3Ј¬јҙAЈҪB-2Ј¬ХвКЗ№Ш
јьЈ¬ИЎЦө·¶О§BЈҫ27Ј¬AЈҫ25¶шОЮЙППЮ(Ц»Ри·ыәПAЈҪB-2)ЎЈўЫЎЎ Лб¶ФMgІ»ЧгЈ¬јо¶ФAlУРУаКұЈ¬УҰОӘA-1ЈҪ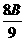 ЎЈИЎЦө·¶О§ФхСщ?Лб¶ФMgІ»ЧгЈ¬өұИ»РиAЈҫ12Ј¬ХвКұBУҰУЙA-1ЈҪ
ЎЈИЎЦө·¶О§ФхСщ?Лб¶ФMgІ»ЧгЈ¬өұИ»РиAЈҫ12Ј¬ХвКұBУҰУЙA-1ЈҪ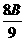 ЛгКҪ¶ш¶ЁЈ¬Ҫ«AЈҫ12ҙъИлЦӘBЈҫ12.375Ј¬№КBөДИЎЦө·¶О§ОӘ27ЈҫBЈҫ1 2.375.¶шMgКЗ·сОӘ27ЈҫAЈҫ12?І»КЗөДЎЈөұBЈј27КұЈ¬AУҰУЙ
ЛгКҪ¶ш¶ЁЈ¬Ҫ«AЈҫ12ҙъИлЦӘBЈҫ12.375Ј¬№КBөДИЎЦө·¶О§ОӘ27ЈҫBЈҫ1 2.375.¶шMgКЗ·сОӘ27ЈҫAЈҫ12?І»КЗөДЎЈөұBЈј27КұЈ¬AУҰУЙ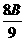 ЈҪA-1ҫц ¶ЁЈ¬јҙ
ЈҪA-1ҫц ¶ЁЈ¬јҙ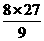 ЈҪA-1өГAЈҪ25Ј¬БоBЈј27Ј¬ФтAЈј25Ј¬AөДИЎЦө·¶О§ОӘ12ЈјAЈј25ЎЈўЬЎЎ Лб¶ФMgУРУаЈ¬јо¶ФAlІ»ЧгКұЈ¬УҰУР
ЈҪA-1өГAЈҪ25Ј¬БоBЈј27Ј¬ФтAЈј25Ј¬AөДИЎЦө·¶О§ОӘ12ЈјAЈј25ЎЈўЬЎЎ Лб¶ФMgУРУаЈ¬јо¶ФAlІ»ЧгКұЈ¬УҰУР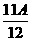 ЈҪB-3Ј¬¶шAЈј12Ј¬BЈҫ27Ј¬ҝЙјыХвЦЦЗйҝцКЗІ»ҝЙДЬөДЎЈ
ЈҪB-3Ј¬¶шAЈј12Ј¬BЈҫ27Ј¬ҝЙјыХвЦЦЗйҝцКЗІ»ҝЙДЬөДЎЈ
35.ИзПВНјОӘөзҪвNaOHИЬТәөДКҫТвНјЈә
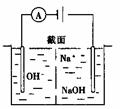
(1)ФЪНјЦРұкіцДЖАлЧУәНЗвСхёщАлЧУөДФЛ¶Ҝ·ҪПтЎЈ
(2)ТСЦӘөзБчұнөД¶БКэКЗ0.6AЈ¬ФтТ»ГлЦУНЁ№эИЬТәҪШГжөДТхЎўСфАлЧУКэ·ЦұрОӘЎЎЎЎЎЎЎЎ Ј¬
ЎЎЎЎЎЎЎЎЎЎЎЎ ЎЈ
(3)РҙіцөзҪвЗвСх»ҜДЖЛ®ИЬТәөД»ҜС§·ҙУҰ·ҪіМКҪЈә
(4)ҙУДЬБҝЧӘ»ҜөДҪЗ¶ИҝҙЈ¬НЁөзКұДЬБҝУЙЎЎЎЎЎЎЎЎЎЎЎЎ ДЬЧӘ»ҜОӘЎЎЎЎЎЎЎЎ ДЬУлЎЎЎЎЎЎЎЎЎЎЎЎ ДЬЎЈФЪЙПКцөзВ·ЦРЈ¬ИфөзФҙөз¶ҜКЖОӘҰЕЈ¬ДЪЧиОӘr Ј¬өзҪвІЫЦРИЬТәөДөИР§өзЧиОӘRЈ¬өзБчұнөД¶БКэОӘIЈ¬өзҪвКұјдОӘtЈ¬ФтХв¶ОКұјдДЪЧӘ»ҜОӘ»Ҝ С§ДЬөДДЬБҝОӘЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЈ
(5)Ҫ«ЦКБҝ·ЦКэОӘ0.052(5.2%)өДNaOHИЬТә1L(ГЬ¶ИОӘ1.06gЎӨcmЈӯ3)УГІ¬өзј«өзҪвЈ¬өұИЬТәЦРNaOHөДЦКБҝ·ЦКэёДұдБЛ0.010(1.0%)КұНЈЦ№өзҪвЎЈФтөзҪвәу
ўЩЎЎ ИЬТәЦРЛщә¬ИЬЦКөДЦКБҝ·ЦКэОӘЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎЎЈ
ўЪЎЎ Сфј«ЙПОціцОпЦКөДОпЦКөДБҝОӘЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЈ
(6)ТСЦӘЗҰРоөзіШідЎў·ЕөзөДЧЬ·ҙУҰКҪОӘЈә
Pb+PbO2+2H2SO4 2PbSO4+2H2O
2PbSO4+2H2O
ЙПМв(5)NaOHИЬТәөзҪвКұИфК№УГЗҰРоөзіШЧчөзФҙЈ¬өзҪв№эіМЦРРоөзіШДЪПыәДБтЛбөДОпЦКөДБҝ ЦБЙЩОӘЎЎЎЎЎЎЎЎЎЎЎЎ ЎЈ
34.ОӘіэИҘ»рБҰ·ўөзХҫөД·ПЖшЦРөД¶юСх»ҜБтЈ¬ҝЙУГМјЛбёЖ»тЗвСх»ҜёЖөДРьЧЗЛ®ИЬТәПҙөУЈ¬·ҙУҰІъОпОӘКҜёа(CaSO4ЎӨ2H2O)ЎЈ
(1)РҙіцЙПКцБҪёц·ҙУҰөД»ҜС§·ҪіМКҪЎЈ
(2)Йи·ПЖш10000m3/hЈ¬ә¬¶юСх»ҜБт0.150%(0ЎжЈ¬1.01ЎБ105Pa),¶юСх»ҜБтөДҫ»»ҜВКОӘ95%Ј¬ОКТ»ЦзТ№РиТӘ¶аЙЩkgМјЛбёЖ?
(3)ФЪ2МвөДМхјюПВГҝМмөГөҪ¶аЙЩkgКҜёа?
33.(1)БЪұҪ¶юјЧЛбЗвјШ(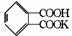 Па¶Ф·ЦЧУЦКБҝОӘ204.2)ҝЙТФУГУЪұк¶ЁNaOHИЬТәөДЕЁ¶ИЈ¬·ҙУҰИзПВЈәKHC8H4O4+NaOH
Па¶Ф·ЦЧУЦКБҝОӘ204.2)ҝЙТФУГУЪұк¶ЁNaOHИЬТәөДЕЁ¶ИЈ¬·ҙУҰИзПВЈәKHC8H4O4+NaOH KNaC8H4O4+H2OЎЈЧјИ·іЖИЎKHC8H4O4ҫ§Ме0.5105gЈ¬ИЬУЪЛ®әујУ Ил·УМӘЦёКҫјБЈ¬УГNaOHИЬТәөО¶ЁЦБИЬТәіКөӯәмЙ«ПыәДNaOH20.00mLЎЈјЖЛгNaOHИЬТәөДОпЦКөДБҝЕЁ¶И(Ҫб№ыұЈБф4О»УРР§КэЧЦ)ЎЈ
KNaC8H4O4+H2OЎЈЧјИ·іЖИЎKHC8H4O4ҫ§Ме0.5105gЈ¬ИЬУЪЛ®әујУ Ил·УМӘЦёКҫјБЈ¬УГNaOHИЬТәөО¶ЁЦБИЬТәіКөӯәмЙ«ПыәДNaOH20.00mLЎЈјЖЛгNaOHИЬТәөДОпЦКөДБҝЕЁ¶И(Ҫб№ыұЈБф4О»УРР§КэЧЦ)ЎЈ
(2)КіҙЧЦРіэҙЧЛбНвЈ¬»№ә¬УРЖдЛыУР»ъЛбЈ¬КіҙЧөДЧЬЛб¶ИТФГҝ1000mLКіҙЧЦРә¬ҙЧЛб(ЖдЛыЛбТІ ХЫЛгЧчҙЧЛб)өДЦКБҝ(g)ұнКҫЈ¬НЁіЈРҙЧчCH3COOH%ЎЈУГТЖТә№ЬТЖИЎКРКЫКіҙЧ50.00mLЈ¬ЦГУЪ2 50mLИЭБҝЖҝЦРЈ¬УГЛ®ПЎКНЦБҝМ¶ИЎЈФЩҙУЦРТЖИЎ25.00mLЈ¬УГЙПРЎМвТСЦӘЕЁ¶ИөДNaOHИЬТәөО¶Ё Ј¬ПыәДјоТәМе»эОӘV(mL)Ј¬РҙіцCH3COOH%өДјЖЛгКҪЎЈ
(3)ТСЦӘ0.1mol/LБЪұҪ¶юјЧЛбИЬТәөДpHҙуУЪ1Ј¬ИЎөИМе»эөДБЪұҪ¶юјЧЛбИЬТәәНДіKOHИЬТә»мәПЈ¬ІвөГ»мәПИЬТәөДpHөИУЪ7Ј¬ФтјоУлЛбөДЕЁ¶ИұИЦө(x)ОӘЎЎЎЎЎЎЎЎЎЎЎЎ (СЎМоПВБРСЎПоұаәЕ)ЎЈ
A.xЈҫ2ЎЎЎЎ B.x=2ЎЎЎЎЎЎ C.2ЈҫxЈҫ1ЎЎ D.x=1 ЎЎE.1ЈҫxЈҫ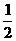 ЎЎЎЎЎЎ
F.x=
ЎЎЎЎЎЎ
F.x=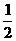
32.ұҫ°ёПа¶Ф·ЦЧУЦКБҝУГТФПВКэҫЭЈәH2O-18.0ЎЎ CaO-56.0ЎЎ CaO2-72.0
№эСх»ҜёЖКЗТ»ЦЦНкИ«ОЮ¶ҫөДСх»ҜОпЈ¬НЁіЈә¬УРІҝ·ЦCaO,ЗТҙшУРКэБҝІ»өИөДҪбҫ§Л®ЎЈОӘ·ЦОцДі №эСх»ҜёЖСщЖ·өДЧйіЙЈ¬ҪшРРБЛИзПВКөСйЈә
ўЩЎЎ іЖИЎ0.270 gСщЖ·Ј¬ЧЖИИК№Ц®НкИ«·ЦҪвЈ¬ЙъіЙCaOЎўO2әНH2OЈ¬өГөҪөДO2ФЪұкЧјЧҙҝцПВМе»эОӘ33.6 mLЎЈ
ўЪЎЎ БнИЎ0.120 gСщЖ·Ј¬ИЬУЪПЎСОЛбЈ¬јУИИЦу·РЈ¬К№ЙъіЙөДH2O2НкИ«·ЦҪвЎЈИ»әуҪ«ИЬТәЦРөДCa2+НкИ«ЧӘ»ҜОӘCaC2O4іБөнЈ¬ҫӯ№эВЛПҙөУәуЈ¬Ҫ«іБөнИЬУЪИИөДПЎБтЛбЈ¬УГ0.02 00 mol/L KMnO4ИЬТәөО¶ЁЈ¬№ІУГИҘ31.0 mL KMnO4ИЬТәЎЈ»ҜС§·ҪіМКҪИзПВЈә
5CaC2O4+2KMnO4+8H2SO4ЈҪK2SO4+2MnSO4+5CaSO4+10CO2Ўь+8H2O
(1)РҙіцCaO2КЬИИ·ЦҪвөД»ҜС§·ҪіМКҪЎЈ
(2)јЖЛгСщЖ·ЦРCaO2өДЦКБҝ·ЦКэЎЈ
(3)јЖЛгСщЖ·ЦРCaO2ЎӨxH2OөДxЦөЎЈ
31.Пт100 mLДі¶юјЫҪрКфMөДЗвСх»ҜОпіОЗеИЬТәЦРјУИл№эБҝөДNaHCO3ИЬТәЈ¬ЙъіЙБЛMCO3 іБөнЈ¬№эВЛЈ¬Ҫ«іБөнЦГУЪЧгБҝөДСОЛбИЬТәЦРЈ¬ФЪұкЧјЧҙҝцПВКХјҜөҪБЛ4.48 LЖшМеЎЈҪ«ВЛТәјУЛ®ПЎКНЦБ250 mLЈ¬ИЎіц25 mLЗЎәГУл20 mLСОЛбНкИ«·ҙУҰЈ¬ФЪұкЧјЧҙҝцПВКХјҜөҪБЛ1.12LЖшМеЎЈ
(1)MөДЗвСх»ҜОпіОЗеИЬТәУлNaHCO3ИЬТә·ҙУҰөД»ҜС§·ҪіМКҪОӘЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЈ
(2)ТӘјЖЛгҪрКфMөДПа¶ФФӯЧУЦКБҝЈ¬ДгИПОӘ»№ұШРиТӘПВБРДДПоКэҫЭ(МоСЎПоКэЧЦ)?
ўЩЎЎ MөДЗвСх»ҜОпИЬТәөДОпЦКөДБҝЕЁ¶И(ЙиОӘ2 mol/L)
ўЪЎЎ MөДМјЛбСОөДЦКБҝ(ЙиОӘ39.4 g)
ўЫЎЎ УлMөДМјЛбСО·ҙУҰөДСОЛбөДОпЦКөДБҝЕЁ¶И(ЙиОӘ0.1 mol/L)
ўЬЎЎ МвЙиМхјюідЧгЈ¬І»РиТӘІ№ідКэҫЭ
(3)ёщҫЭДгөДСЎФсЈ¬КФјЖЛгҪрКфMөДПа¶ФФӯЧУЦКБҝәНјУИлөДNaHCO3ИЬТәЦРЛщә¬NaHCO3өДЦК БҝЎЈ
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com