
题目列表(包括答案和解析)
5. 下列叙述正确的是( )
A.H2与H的核外电子数相同
B.Cl和Cl-核外电子层数不同
C.在CS2、PCl3中各原子最外层均能达到8电子的稳定结构
D.Ar原子的结构示意图为:
解析:H2是分子,核外共有2个电子,H是原子,核外只有1个电子,A错;Cl和Cl-都有3个电子层,B错;根据CS2和PCl3的成键情况可推出C正确;而Ar原子的结构示意图应为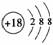 ,D错。
,D错。
答案:C
4.已知自然界中铱(Ir)有两种质量数分别为191和193的核素,而铱元素的相对原子质量为192.22。这两种同位素的原子个数比应为( )
A.39∶61 B.61∶39 C.1∶1 D.39∶11
解析:采用十字交叉法:
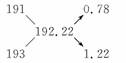
则两种同位素原子的个数比为0.78∶1.22=39∶61。
答案:A
3.已知元素X、Y的核电荷数分别是a和b,它们的离子Xm+和Yn-的核外电子排布相同,则下列关系式中正确的是( )
A.a=b+m+n B.a=b-m+n C.a=b+m-n D.a=b-m-n
解析:在原子中,核电荷数等于核外电子数;在阳离子中,核电荷数减去离子所带电荷数等于核外电子数;在阴离子中,核电荷数加上离子所带电荷数等于核外电子数。因为Xm+和Yn-具有相同的核外电子排布,所以,Xm+和Yn-具有相同的核外电子数,aXm+的核外电子数等于a-m,bYn-的核外电子数为:b+n,则:a-m=b+n。
答案:A
2. U是重要的核工业原料,在自然界的丰度很低。U的浓缩一直为国际社会关注。下列有关U说法正确的是( )
A.U原子核中含有92个中子 B.U原子核外有143个电子
C.U与U互为同位素 D.U与U互为同素异形体
解析:U的中子数为235-92=143,其核外电子数为92,故A、B均为错误答案;同素异形体是指同一元素形成的不同单质,U和U应互为同位素。
答案:C
1.甲、乙两元素原子的L层电子数都是其他层电子总数的2倍。下列推断正确的是( )
A.甲与乙处于同一周期 B.甲与乙处于同一主族
C.甲与乙的单质都是原子晶体 D.甲与乙的原子序数之和为偶数
解析:本题主要信息是原子的电子排布特点。可以先根据核外电子排布规律确定可能的元素名称,再确定位置,从而推断单质的性质等。
L层最多可有8个电子,当其他层共有4个电子时符合题意,根据核外电子排布规律,Mg符合条件;当L层未填满电子时,K层的2个电子已填入,此时L层应有4个电子,碳符合条件,则甲、乙指的是碳和镁,D选项符合题意。
答案:D
7.(原创题)实验室制Cl2时,尾气用碱液吸收,发生Cl2+2OH-===Cl-+ClO-+H2O可以清除污染,将Cl2通入热的氢氧化钠溶液中也发生类似的反应,但产物更复杂,某同学在一次实验中测得反应后溶液中只含有三种溶质其中两种是NaClO2和NaClO4,你推测溶液中含有的另一种溶质是 _,如果溶液中ClO和ClO的物质的量浓度之比是1∶2,试写出该反应的离子方程式: 。
解析:本题根据Cl2尾气处理的反应,利用氧化还原反应中元素得失电子情况可以写出反应的离子方程式。
答案:NaCl 10Cl2+20OH-===17Cl-+ClO+2ClO+10H2O
6. A、B、C、D、E均为可溶于水的固体,组成它们的离子有
|
阳 离 子 |
Na+ Mg2+ Al3+ Ba2+ |
|
阴 离 子 |
OH- Cl- CO SO HSO |
分别取它们的水溶液进行实验,结果如下:
①A溶液与B溶液反应生成白色沉淀,沉淀可溶于E溶液;
②A溶液与C溶液反应生成白色沉淀,沉淀可溶于E溶液;
③A溶液与D溶液反应生成白色沉淀,沉淀可溶于盐酸;
④B溶液与适量D溶液反应生成白色沉淀,加入过量D溶液,沉淀量减少,但不消失。
据此推断它们是:
A ;B ;C ;D ;E 。
解析:解决本题的突破口在于④即B中加适量D有白色沉淀生成,加过量D沉淀量减少,所以B中含Al3+,D中含OH-,但加过量D时沉淀并不消失,D不能为NaOH,只能为Ba(OH)2,从而推断出B为Al2(SO4)3。结合①、②、③,A可和三种物质生成沉淀,推断A只能为Na2CO3。①、②中的沉淀均可溶于E溶液,E中的阴离子应为HSO,结合生成的白色沉淀能溶于E,阳离子可能为Na+或Mg2+,所以E为NaHSO4或Mg(HSO4)2。熟记溶解性表是解决本题的关键,也是解决离子共存问题、书写离子方程式等问题的必备知识。
答案:Na2CO3 Al2(SO4)3 MgCl2 Ba(OH)2 NaHSO4[或Mg(HSO4)2]
5.现有五种离子化合物A、B、C、D和E,都是由右表中离子形成的:
为鉴别它们,分别完成以下表实验,其结果是
|
阳离子 |
Ag+ Ba2+ Al3+ |
|
阴离子 |
OH- Cl- SO |
a.B和D都不溶于水,也不溶于酸;
b.A溶于水后,与上述某阳离子反应可生成B,且A溶液与过量氨水反应生成白色沉淀;
c.C溶于水后,与上述某阳离子反应可生成D,且C溶液与过量氨水反应生成白色沉淀;
d.E溶于水后,与上述某阴离子反应可生成B;
e.A溶液与适量E溶液反应生成沉淀,再加入过量E溶液,沉淀量减少,但不消失。
请根据上述实验结果,填空:
(1)写出化合物的化学式A ,C ,D ,E 。
(2)A溶液与过量的E溶液反应后,最终得到的沉淀的化学式是 。
解析:解答本题应把局部小规模推断与整体综合判断相结合。①不溶于水,也不溶于酸的物质为BaSO4和AgCl;②、③中可与氨水生成白色沉淀的A和C应在Al2(SO4)3和AlCl3中选出;④E中必含有Ba2+;⑤能满足题述条件的只有Al2(SO4)3和Ba(OH)2之间的反应。A为Al2(SO4)3,E为Ba(OH)2。当Ba(OH)2适量时,发生反应Al2(SO4)3+3Ba(OH)2===2Al(OH)3↓+3BaSO4↓;而一旦Ba(OH)2过量,前面生成的Al(OH)3沉淀就会发生溶解,而BaSO4的量不受影响,反应可表示为Al(OH)3+OH-===AlO+2H2O。结合前面所做推断可确定出B为BaSO4,C为AlCl3,D为AgCl。
答案:Al2(SO4)3 AlCl3 AgCl Ba(OH)2 (2)BaSO4
4.(2009·全国Ⅱ理综,29)现有A、B、C、D、E、F六种化合物,已知它们的阳离子有K+、Ag+、Ca2+、Ba2+、Fe2+、Al3+,阴离子有Cl-、OH-、CH3COO-、NO、SO、CO,现将它们分别配成0.1 mol·L-1的溶液,进行如下实验:
①测得溶液A、C、E呈碱性,且碱性为A>E>C;
②向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
③向D溶液中滴加Ba(NO3)2溶液,无明显现象;
④向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色。
根据上述实验现象,回答下列问题:
(1)实验②中反应的化学方程式是 ;
(2)E溶液是 ,判断依据是 ;
(3)写出下列四种化合物的化学式:A 、C 、D 、F 。
解析:由①中碱性强弱顺序可知A是碱,E是碳酸盐,C是醋酸盐;而所给六种阳离子可以与CO形成可溶性盐的只有K+,所以E是K2CO3。由②中现象可知B中有Ag+,则应是AgNO3。由③中现象知D中无CO和SO。由④中现象可知F中有Fe2+。由题意知六种化合物均是可溶性的,A是碱,则应是Ba(OH)2。C是强碱弱酸盐,则为(CH3COO)2Ca。D中无CO和SO,则F中有SO,F为FeSO4,D是AlCl3。
答案:(1)AgNO3+NH3·H2O===AgOH↓+NH4NO3 AgOH+2NH3·H2O===Ag(NH3)2OH+2H2O (2)碳酸钾 由①中碱性强弱的顺序可知E是碳酸盐。六种阳离子中可以与碳酸根形成可溶性盐的只有钾离子,所以E是碳酸钾 F的离子方程式为 。
a(OH)2 (CH3COO)2Ca AlCl3 FeSO4
3.(2009·江苏单科,7)在下列各溶液中,离子一定能大量共存的是( )
A. 强碱性溶液中:K+、Al3+、Cl-、SO
B.含有0.1 mol·L-1 Fe3+的溶液中:K+、Mg2+、I-、NO
C.含有0.1 mol·L-1 Ca2+的溶液中:Na+、K+、CO、Cl-
D.室温下,pH=1的溶液中,Na+、Fe3+、NO、SO
解析:A项,强碱性溶液中有大量OH-,Al3+不能大量共存;B项,Fe3+与I-不能大量共存;C项,Ca2+与CO因形成沉淀而不能大量共存;D项正确。
答案:D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com