
题目列表(包括答案和解析)
1.(2009·重庆理综,6)材料与化学密切相关,表中对应关系错误的是( )
|
选项 |
材 料 |
主要化学成分 |
|
A |
刚玉、金刚石 |
三氧化二铝 |
|
B |
大理石、石灰石 |
碳酸钙 |
|
C |
普通水泥、普通玻璃 |
硅酸盐 |
|
D |
沙子、石英 |
二氧化硅 |
解析:A项,刚玉的主要化学成分为三氧化二铝,而金刚石的主要化学成分为碳。
答案:A
6. 已知甲和I、L、M均为常见的单质,I在常温下为气体,L、M为金属;气体K的水溶液显碱性;A是由前20号元素组成的阴、阳离子个数比为1∶1的离子化合物,且阴离子含有14个电子;乙是一种红棕色的粉末,G为白色胶体沉淀,D在常温下是无色液体,C的溶液常用于在实验室检验E。各物质之间的转化关系如右图所示(部分物质在图中没有列出),已知CaC2+2H2O―→Ca(OH)2+C2H2↑。

请根据要求填空:
(1)A的化学式为__________,J的化学式为_______________________________________。
(2)反应①的化学方程式为______________________________________________________。
(3)反应②的化学方程式为______________________________________________________。
(4)J→G的离子方程式为_______________________________________________________。
解析:本题的“突破口”是“乙是一种红棕色粉末”,可知乙是Fe2O3,由L、M为金属单质可知L、M分别是Al、Fe,推出I、J、D分别为H2、Na[Al(OH)4]、H2O,由G为白色胶体沉淀可知G为Al(OH)3,由气体K的水溶液显碱性可知K为NH3;因为H与Fe2O3反应生成Fe,可知H有还原性,可推出甲、H、E分别为C、CO、CO2,故B中一定有C、H元素,可能含有氧元素,由C的溶液常用于检验E(CO2)可知C为Ca(OH)2,A为CaC2,B为C2H2,N为铵盐。
答案:(1)CaC2 Na[Al(OH)4]
(2)H2O(g)+CCO+H2
(3)2Al+Fe2O32Fe+Al2O3
(4)CO2+[Al(OH)4]-===Al(OH)3↓+HCO
5.根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
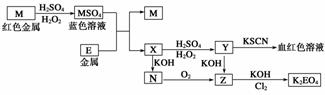
(1)写出M溶于稀H2SO4和H2O2混合液的化学方程式:
________________________________________________________________________。
(2)某同学取X的溶液,酸化后加入KI、淀粉溶液,变为蓝色。写出与上述变化过程相关的离子方程式:_________________、________________________________________________。
(3)写出N转化为Z的现象及化学方程式:_________________________________________
________________________________________________________________________。
(4)写出Cl2将Z氧化为K2EO4的化学方程式:
________________________________________________________________________。
解析:分析本题应以M为红色金属(Cu)和Y与KSCN溶液反应变血红色着手。从转化图中的转化关系和现象可知,E、X、Y、N、Z、K2EO4中均含有铁元素,且Y为Fe3+,则Z为Fe(OH)3,N为Fe(OH)2,X为FeSO4,E为Fe。确定相关物质后,即可完成各问题。
答案:(1)Cu+H2O2+H2SO4===CuSO4+2H2O (2)4Fe2++O2+4H+===4Fe3++2H2O 2Fe3++2I-===2Fe2++I2 (3)白色沉淀迅速转化为灰绿色,最后变为红褐色, 4Fe(OH)2+O2+2H2O===4Fe(OH)3 (4)10KOH+3Cl2+2Fe(OH)3===2K2FeO4+6KCl+8H2O
4. A、B、C、D、E、F是中学化学中常见的物质,它们之间转化关系如图所示。其中A、B为单质,F为白色沉淀,D为气体。
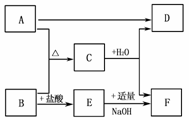
(1)若D的水溶液显弱酸性,则
A是__________,B是__________,C是____________,
D是__________,E是__________,F是____________。
(2)若D的水溶液显弱碱性,则
A是__________,B是__________,C是____________,
D是__________,E是__________,F是____________。
解析:E与NaOH反应生成白色沉淀F,则F必是氢氧化物,常见的白色氢氧化物沉淀有Mg(OH)2和Al(OH)3,进一步推知E为MgCl2或AlCl3,B为Mg或Al,A为非金属单质。又因为C能与H2O反应产生气体同时生成Al(OH)3或Mg(OH)2,则C与H2O的反应是水解反应。显碱性的气体常见的只有NH3,可确定C为Mg3N2,A为N2,B为Mg。当D为酸性气体时,且是水解产生的,则C同样是与Mg3N2相类似的盐,常见的为Al2S3,推知A为S,B为Al。
答案:(1)S Al Al2S3 H2S AlCl3 Al(OH)3 (2)N2 Mg Mg3N2 NH3 MgCl2
Mg(OH)2
3.根据下图所示的关系

确定A、B、C、D、E、F的化学式,A为__________,B为__________,C为__________,D为________,E为________,F为________。
解析:从最初条件看,框图很模糊,直接得不出结论,但找到题眼:“红褐色固体F”、“黑色晶体B”,就可迅速得出红褐色固体F是Fe(OH)3,从而得出A为Fe,B为Fe3O4,C为FeSO4,D为Fe2(SO4)3,E为Fe(OH)2。
答案:Fe Fe3O4 FeSO4 Fe2(SO4)3 Fe(OH)2 Fe(OH)3
2.A、B、C为中学常见单质,其中一种为金属;通常情况下,A为固体,B为液体,C为气体。D、E、F、G、H、X均为化合物,其中X是一种无氧强酸、E为黑色固体,H在常温下为液体。它们之间的转化关系如下图所示(其中某些反应条件和部分反应产物已略去)。

(1)写出化学式:A______、D______、E______、X________。
(2)在反应①-⑦中,不属于氧化还原反应的是________(填编号)。
(3)反应⑥的离子方程式为:_____________________________________________________;
D除了可与F反应得到一种血红色溶液外,还可与某有机物反应生成紫色物质,该有机物是______________(填名称)。
(4)反应⑦的化学方程式为_____________________________________________________;
该反应中每消耗0.3 mol的A,可转移电子______mol。
(5)写出D的溶液与小苏打溶液反应的离子方程式:_________________________________。
解析:依据题意可知A应为金属,B为液溴,A+Br2―→D,D+A―→G,说明A是一种变价金属,故为Fe,Fe与C生成黑色固体可推出C为O2,E+X―→D+G+H,说明X为HBr。
答案:(1)Fe FeBr3 Fe3O4 HBr (2)③⑥ (3)Fe3++3SCN-Fe(SCN)3 苯酚
(4)3Fe+4H2O(g)Fe3O4+4H2 0.8 (5)Fe3++3HCO===Fe(OH)3↓+3CO2↑
1.由短周期元素组成的单质A、B、C和甲、乙、丙、丁、戊五种化合物有如图所示的转换关系,甲是工业上制取A的主要原料。请回答:
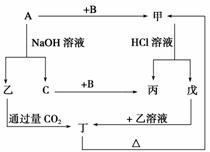
(1)写出下列物质的化学式:
A__________,乙__________。
(2)写出甲物质在工业上的任意两种主要用途_____________________________________
________________________________________________________________________。
(3)写出下列变化的化学方程式:
①A与NaOH溶液反应的化学方程式:____________________________________________;
②乙与过量CO2反应的离子方程式______________________________________________;
③戊溶液与乙溶液混合的离子方程式_____________________________________________。
解析:本题的“突破口”是单质A与NaOH溶液反应,生成单质C,则C为H2,A可能是铝或硅,而A和B的产物甲能与盐酸反应,推知A为Al,B为O2。
答案:(1)Al Na[Al(OH)4] (2)作耐高温材料;制取铝单质
(3)①2Al+2NaOH+6H2O===2Na[Al(OH)4]+3H2↑
②[Al(OH)4]-+CO2===Al(OH)3↓+HCO
③Al3++3[Al(OH)4]-===4Al(OH)3↓
7.2 g水。该样品的结晶水质量为________g,化学式为________;
(2)某同学以氮气代替氢气,并用上述全部或部分仪器来测定碱式碳酸铜的组成,你认为是否可行?请说明理由。
解析:(1)①与H2反应的化学方程式,利用氧化还原反应原理,把金属Cu还原出来,碳元素变成CO2,氢元素变成水。
②仪器连接时,洗气瓶要“长进短出”,其中水是除去HCl气体并观察H2生成速率的。
③残留固体一定是Cu,则n(Cu)==0.2(mol),根据题意,n(CO2)=n(CuCO3)=
=0.1(mol),
所以,m(CuCO3)=123.5×n(CuCO3)=12.35 (g),
m[Cu(OH)2]=97.5×[n(Cu)-n(CuCO3)]=9.75(g),m(结晶水)
=23.9-12.35-9.75=1.8(g)。该碱式碳酸铜化学式为CuCO3·Cu(OH)2·H2O。
(2)根据xCuCO3·yCu(OH)2·zH2O(x+y)CuO+xCO2↑+(y+z)H2O↑,依据元素守恒和质量守恒,即可得出答案。
答案:(1)①xCuCO3·yCu(OH)2·zH2O+(x+y)H2(x+y)Cu+xCO2+(x+2y+z)H2O
②a―→kj―→gf(或hi)―→de(或ed)―→hi(或gf)―→bc(或cb)―→l
③1.8 CuCO3·Cu(OH)2·H2O
(2)可以。 根据反应xCuCO3·yCu(OH)2·zH2O(x+y)CuO+xCO2↑+(y+z)H2O↑
依据碱式碳酸铜样品、CuO、CO2和H2O质量(或其中任意三个量),即可计算出其组成。
3. (2009·宁夏理综,26)碱式碳酸铜可表示为:xCuCO3·yCu(OH)2·zH2O,测定碱式碳酸铜组成的方法有多种。
(1)现采用氢气还原法,请回答如下问题:
①写出xCuCO3·yCu(OH)2·zH2O与氢气反应的化学方程式________________________________________________________________________;
②实验装置用下列所有仪器连接而成,按氢气流方向的连接顺序是(填入仪器接口字母编号):
(a)―→( )( )―→( )( )―→( )( )―→( )( )―→( )( )―→(l)

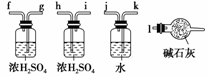
③称取23.9 g某碱式碳酸铜样品,充分反应后得到12.7 g残留物,生成4.4 g二氧化碳和
2.(2009·广东单科,21)三草酸合铁酸钾晶体K3[Fe(C2O4)3]·3H2O可用于摄影和蓝色印刷。某小组将无水三草酸合铁酸钾在一定条件下加热分解,对所得气体产物和固体产物进行实验和探究。请利用实验室常用仪器、用品和以下限选试剂完成验证和探究过程。
限选试剂:浓硫酸、1.0 mol·L-1 HNO3溶液、1.0 mol·L-1盐酸、1.0 mol·L-1 NaOH溶液、3%H2O2溶液、0.1 mol·L-1 KI溶液、0.1 mol·L-1 CuSO4溶液、20% KSCN溶液、澄清石灰水、氧化铜、蒸馏水。
(1)将气体产物依次通过澄清石灰水(A)、浓硫酸、灼热氧化铜(B)、澄清石灰水(C),观察到A、C中澄清石灰水都变浑浊,B中有红色固体生成,则气体产物是________。
(2)该小组同学查阅资料后推知,固体产物中,铁元素不可能以三价形式存在,而盐只有K2CO3。验证固体产物中钾元素存在的方法是________,现象是________________________________________________________________________。
(3)固体产物中铁元素存在形式的探究。
①提出合理假设
假设1:__________________________________________________________________;
假设2:___________________________________________________________________;
假设3:________________________________________________________________。
②设计实验方案证明你的假设
③实验过程
根据②中方案进行实验。按下表的格式写出实验步骤、预期现象与结论。
|
实验步骤 |
预期现象与结论 |
|
步骤1: |
|
|
步骤2: |
|
|
步骤3: |
|
|
…… |
|
解析:(1)根据A中石灰水变浑浊,知有CO2气体,B中有红色固体生成,说明CuO被还原,C中石灰水变浑浊,可知B中CuO被CO还原。
(3)因为题目中说明铁不以三价存在,只能是以二价铁或单质形式,或两者混合物存在。
步骤1:利用K2CO3的溶解性,除去K2CO3;
步骤2:利用铁能置换出Cu,而FeO不能置换出Cu来检验是否含铁单质;
步骤3:利用盐酸酸化分离出FeO,再用H2O2氧化,利用KSCN是否变色,来验证固体中是否含FeO。
答案:(1)CO和CO2 (2)焰色反应 透过蓝色钴玻璃观察到紫色火焰 (3)①全部为铁单质 全部为FeO 同时存在铁单质和FeO
③
|
实验步骤 |
预期现象与结论 |
|
步骤1:取适量固体产物于试管中,加入足量蒸馏水,充分振荡使K2CO3完全溶解。分离不溶固体与溶液,用蒸馏水充分洗涤不溶固体。 |
固体产物部分溶解。 |
|
步骤2:向试管中加入适量CuSO4溶液,再加入少量上述不溶固体,充分振荡。 |
(1)若蓝色溶液颜色及加入的不溶固体无明显变化,则假设2成立。 (2)若蓝色溶液颜色明显改变,且有暗红色固体物质生成,则证明有铁单质存在。 |
|
步骤3:继续步骤2中的(2),进行固液分离,用蒸馏水洗涤固体至洗涤液无色。取少量固体于试管中,滴加过量HCl后,静置,取上层清液,滴加适量H2O2,充分振荡后滴加KSCN。 |
结合步骤2中的(2); (1)若溶液基本无色,则假设1成立。 (2)若溶液呈血红色,则假设3成立。 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com