
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
8.(09-10ЁЄИЃНЈИЃжнАЫжаИпЖўЯТЦкжа) ЯТСаУшЪіжаЃЌДэЮѓЕФЪЧ
ЁЁЁЁЁЁ AЃЎЭљЯТЫЎЕРжаЧуЕЙСђЫсЭШмвКЃЌЛсНјвЛВНМгПьЬњжЦЙмЕРЕФИЏЪД
ЁЁЁЁЁЁ BЃЎУОгыЯЁбЮЫсЗДгІОчСвЃЌМгШыДзЫсФЦОЇЬхПЩвдМѕТ§ЗДгІЫйТЪ
ЁЁЁЁЁЁ CЃЎЕчНтБЅКЭЪГбЮЫЎжЦТШЦјЪБгУЬњзїбєМЋ
ЁЁЁЁЁЁ DЃЎЕчНтЗЈОЋСЖДжЭЃЌгУДПЭзївѕМЋ
7.(09-10ЁЄИЃНЈИЃжнАЫжаИпЖўЯТЦкжа) pHЃНaЕФФГЕчНтжЪШмвКжаЃЌВхШыСНжЇЖшадЕчМЋЃЌЭЈжБСїЕчвЛЖЮЪБМфКѓЃЌШмвКЕФpH<aЃЌдђИУЕчНтЪЧ
ЁЁЁЁЁЁ AЃЎNaOHЁЁ BЃЎHCl CЃЎH2SO4ЁЁ DЃЎNa2SO4
6.(09-10ЁЄИЃНЈИЃжнАЫжаИпЖўЯТЦкжа) ЕчНтЯЁH2SO4ЁЂCu(NO3)2ЁЂNaClЕФЛьКЯвКЃЌзюГѕвЛЖЮЪБМфвѕМЋКЭбєМЋЩЯЗжБ№ЮіГіЕФЮяжЪЗжБ№ЪЧ
ЁЁЁЁЁЁ AЃЎH2КЭCl2ЁЁ ЁЁЁЁ BЃЎCuКЭCl2 ЁЁЁЁ CЃЎH2КЭO2ЁЁ ЁЁЁЁ DЃЎCuКЭO2
5.(09-10ЁЄИЃНЈИЃжнАЫжаИпЖўЯТЦкжа) ДгЛЏбЇдРэКЭОМУРћвцНЧЖШЗжЮіЃЌЯТСаДгКЃЫЎжаЬсШЁУОЕЅжЪЕФЗНЗЈзюПЩааЕФЪЧD
4.(09-10ЁЄеуНЖЋбєжабЇИпЖўЯТЦкжа) 23ЃЎЯТСаЪЧАЎЕЯЩњЕчГиЗжБ№дкГфЕчКЭЗХЕчЪБЗЂЩњЕФЗДгІЃК
Fe+ NiO2+2H2O ЁЁFe(OH)2+Ni(OH)2ЃЌЯТСаИУаюЕчГиЭЦЖЯДэЮѓЕФЪЧЁЁЁЁЁЁ (ЁЁЁЁЁЁ )
ЁЁFe(OH)2+Ni(OH)2ЃЌЯТСаИУаюЕчГиЭЦЖЯДэЮѓЕФЪЧЁЁЁЁЁЁ (ЁЁЁЁЁЁ )
A.ЗХЕчЪБЃЌFeВЮгыИКМЋЗДгІЃЌNiO2ВЮгые§МЋЗДгІ
B.ГфЕчЪБЃЌвѕМЋЩЯЕФЕчМЋЗДгІЪНЮЊЃКFe(OH)2 + 2e- = Fe + 2OH-
C.ЗХЕчЪБЃЌЕчНтжЪШмвКжаЕФвѕРызгЯђе§МЋЗНЯђвЦЖЏ
D.аюЕчГиЕФЕчМЋБиаыНўШыФГжжМюадЕчНтжЪШмвКжаЁЁ
3.(09-10ЁЄИЃНЈИЃжнАЫжаИпЖўЯТЦкжа) Фјяг(Ni-Cd)ПЩГфЕчЕчГидкЯжДњЩњЛюжагаЙуЗКгІгУЃЌЫќЕФГфЗХЕчЗДгІАДЯТЪННјааЃКCd(OH)2+2Ni(OH)2  ЁЁCd+2NiO(OH)+2H2OЃЌИУЕчГиЗХЕчЪБЕФИКМЋВФСЯЪЧ
ЁЁCd+2NiO(OH)+2H2OЃЌИУЕчГиЗХЕчЪБЕФИКМЋВФСЯЪЧ
ЁЁЁЁЁЁ AЃЎCd(OH)2ЁЁ ЁЁЁЁ BЃЎCdЁЁЁЁЁЁ CЃЎNi(OH)2ЁЁЁЁ ЁЁ DЃЎNiO(OH)
2.(09-10ЁЄеуНЖЋбєжабЇИпЖўЯТЦкжа) 3ЃЎдкРэТлЩЯВЛФмгУгкЩшМЦдЕчГиЕФЛЏбЇЗДгІЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
AЃЎHCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l) ЁЁBЃЎ2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)ЁЁЁЁЁЁЁЁ ЁЁ
CЃЎ2FeCl2+Cl2=2FeCl3ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁDЃЎ3Fe+8HNO3(ЯЁ)=3Fe(NO3)2+2NO+4H2OЁЁ
1.(09-10ЁЄИЃНЈИЃжнАЫжаИпЖўЯТЦкжа) зАжУШчЭМЃЌЭЈЕчКѓЃЌЗЂЯжCuМЋИННќШмвКРЖЩЋМгЩюЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ
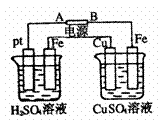 AЃЎAМЋЮЊИКМЋЃЌCuЮЊбєМЋЁЁ
AЃЎAМЋЮЊИКМЋЃЌCuЮЊбєМЋЁЁ
BЃЎзѓЩеБШмвККЭгвЩеБШмвКpHЖМБфаЁ
CЃЎзѓЩеБPtМЋКЭгвЩеБFeМЋЕФЕчНтВњЮяЮяжЪЕФСПжЎБШЮЊ1ЁУ1
DЃЎзѓЩеБШмвКХЈЖШБфДѓЃЌгвЩеБШмвКХЈЖШВЛБф
23ЃЎ(13Зж)ЯТБэЪЧЪЕбщЪвжЦБИЦјЬхЕФгаЙиФкШнЃК
|
БрКХ |
ЪЕбщФкШн |
ЪЕбщдРэ |
ЦјЬхЗЂЩњзАжУ |
|
Ђй |
жЦбѕЦј |
H2O2ЁњO2 |
ЁЁ |
|
Ђк |
жЦАБЦј |
NH4ClЁњNH3 |
ЁЁ |
|
Ђл |
жЦТШЦј |
HClЁњCl2 |
ЁЁ |
ЁЁ (1)ЩЯЪіЦјЬхжаЃКДгжЦБИЙ§ГЬПДЃЌБиаыбЁдёКЯЪЪЕФбѕЛЏМСВХФмЪЕЯжЕФЪЧЁЁЁЁЁЁЁЁ (ЬюЦјЬхЕФЛЏбЇЪНЃЌЯТЭЌЁЃ)ЃЛДгЗДгІдРэПДЃЌУїЯдВЛЭЌгкЦфЫћСНжжЦјЬхЕФЪЧЁЁЁЁЁЁЁЁ .
ЁЁ (2)ИљОнБэжаЫљСаЪЕбщдРэЃЌДгЯТСазАжУжабЁдёКЯЪЪЕФЦјЬхЗЂЩњзАжУЃЌНЋЦфБрКХЬюШыЩЯБэжаЕФПеИёжаЁЃ
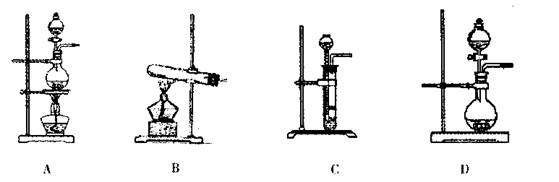
ЁЁ (3)ШєгУЩЯЪіжЦБИO2ЕФзАжУжЦБИNHЁЃЃЌдђбЁдёЕФЪдМСЮЊЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (4)жЦБИC12ашгУ8 molЁЄL-1ЕФбЮЫс100mLЃЌЯжгУ12 molЁЄL-1ЕФбЮЫсРДХфжЦЁЃ
ЂйЮЊЬсИпХфжЦЕФОЋШЗЖШЃЌСПШЁХЈбЮЫсЕФвЧЦїПЩбЁгУЯТСаЕФЁЁЁЁ (ЬюађКХ)

ЂкХфжЦЙ§ГЬжаЃЌГ§ЩЯЭМЫљСавЧЦїЭтЃЌЛЙашвЊЕФвЧЦїгаЁЁЁЁ ЁЁЁЁЁЂЁЁ ЁЁЁЁЁЁЁЂЁЁЁЁЁЁЁЁ ЁЃ
ЂлШєБъЖЈЫљХфбЮЫсЕФХЈЖШЪЧЗёзМШЗЃЌГЃВЩгУЕФЪЕбщЗНЗЈУћГЦЪЧЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (5)ШєгУХХПеЦјЗЈЪеМЏCl2ЃЌдкЯТСаЗНПђФкЛГіЦјЬхЪеМЏзАжУЭМЁЃ
22ЃЎ(10Зж)юбБЛГЦЮЊМЬЬњЁЂТСжЎКѓЕФЕкШ§Н№ЪєЁЃШчЯТЭМЫљЪОЃЌНЋюбГЇЁЂТШМюГЇКЭМзДМГЇзщГЩВњвЕСДПЩвдДѓДѓЬсИпзЪдДРћгУТЪЃЌМѕЩйЛЗОГЮлШОЁЃ
ЁЁЁЁЁЁ ЧыЬюаДЯТСаПеАзЃК
ЁЁ (1)ЕчНтЪГбЮЫЎЪБЃЌзмЗДгІЕФРызгЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
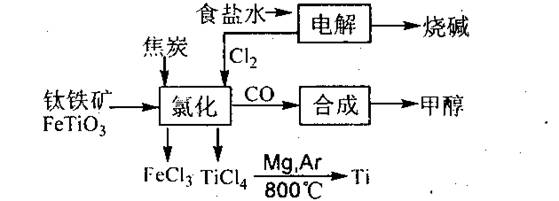
ЁЁ (2)аДГіюбЬњПѓОТШЛЏЗЈЕУЕНЫФТШЛЏюбЕФЛЏбЇЗНГЬЪНЃК
ЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЁЁ (3)вбжЊЃКЂйЃЎMg(s)+Cl2(g)=MgC12(s)ЁЁ ЁїH=-641kJЁЄmol-1
ЁЁЁЁЁЁ ЁЁЁЁ ЂкTi(s)+2C12(g)=TiCl4(s)ЁЁ ЁїH=-770kJЁЄmol-1
ЁЁЁЁ ЁЁЁЁ дђ2Mg(s)+TiCl4(s)=2MgCl2(s)ЪЎTi(s)ЁЁ ЁїH=ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
|
ЁЁЁЁЁЁ ЁЁЁЁ ЗДгІ2Mg(s)+TiCl4(s)ЁЁЁЁ 2MgCl2(s)+Ti(s)дкArЦјЗежаНјааЕФРэгЩЪЧ
ЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЁЁ (4)вдМзДМЁЂПеЦјЁЂЧтбѕЛЏМиШмвКЮЊдСЯЃЌЪЏФЋЮЊЕчМЋПЩЙЙГЩШМСЯЕчГиЁЃИУЕчГижаИКМЋЩЯЕФЕчМЋЗДгІЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com