
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
2£Ææðπ˙Õ‚◊ ¡œ±®µ¿£¨‘⁄“ª÷÷π≤…˙øÛ--∂¿æ” Ø÷–£¨≤È√˜”–…–Œ¥√¸√˚µƒ116∫≈‘™Àÿ£¨≈–∂œ116∫≈‘™Àÿ”¶Œª”⁄÷Ð∆⁄±Ì÷–µƒ(°°)
A£Æµ⁄6÷Ð∆⁄¢ÙA◊°°°°°°B£Æµ⁄7÷Ð∆⁄¢˜◊Â
C£Æµ⁄7÷Ð∆⁄¢ˆA◊°° D£Æµ⁄8÷Ð∆⁄¢ˆA◊Â
Ω‚Œˆ£∫µ⁄7÷Ð∆⁄œ°”–∆¯Ã‘≠◊”–Ú ˝Œ™118£¨‘Ú118£≠116£Ω2£¨À˘“‘∏√‘™Àÿ”¶Œª”⁄µ⁄7÷Ð∆⁄¢ˆA ◊°£
¥∞∏£∫C
1£Æ(2009°§∞≤ª’ ¶¥Û∏Ω÷–)Ω ÙÓ—∂‘Ó∫ŒÞ∂æ«“”–∂Ë–‘£¨ƒÐ”κ°»‚∫Õπ«˜¿…˙≥§‘⁄“ª∆£¨“Ú∂¯”–°∞…˙ŒÔΩ Ù°±÷Æ≥∆°£œ¬¡–”–πÿTi∫ÕTiµƒÀµ∑®÷–’˝»∑µƒ «(°°)
A.Ti∫ÕTi‘≠◊”÷–æ˘∫¨”–22∏ˆ÷–◊”
B.Ti∫ÕTi∫ÀÕ‚æ˘”–4∏ˆµÁ◊”≤„
C£Æ∑÷±”…Ti∫ÕTi◊È≥…µƒΩ ÙÓ—µ•÷ ª•≥∆Œ™Õ¨∑÷“ÏππÃÂ
D.Ti”ÎTiŒ™Õ¨“ª∫ÀÀÿ
Ω‚Œˆ£∫Ti∫ÕTi‘≠◊”÷–À˘∫¨÷–◊” ˝∑÷±Œ™26°¢28£¨AœÓ¥ÌŒÛ£ªTi∫ÕTi‘≠◊”À˘∫¨µƒ÷ ◊” ˝œýÕ¨£¨∫ÀÕ‚µÁ◊” ˝œýÕ¨£¨µÁ◊”≤„ ˝œýÕ¨£¨BœÓ’˝»∑£ªÕ¨∑÷“Ïππà«÷∏∑÷◊” ΩœýÕ¨£¨Ω·ππ≤ªÕ¨µƒªØ∫œŒÔ£¨CœÓ¥ÌŒÛ£ªTi∫ÕTi‘≠◊”µƒ÷ ◊” ˝œýÕ¨£¨÷–◊” ˝≤ªÕ¨£¨ «Õ¨“ª÷÷‘™Àÿµƒ≤ªÕ¨∫ÀÀÿ£¨DœÓ¥ÌŒÛ°£
¥∞∏£∫B
22£Æ(2009°§∏£Ω®æÌ)ƒ≥—–æø–‘—ßœ∞–°◊ÈΩË÷˙A-Dµƒ“«∆˜◊∞÷√ÕÍ≥…”–πÿ µ—È°£
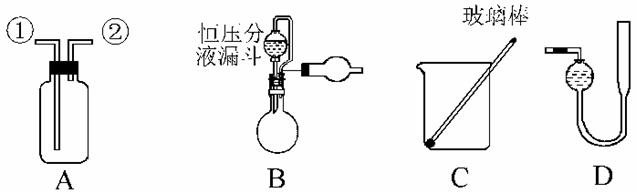
[ µ—È“ª] ’ºØNO∆¯Ã°£
(1)”√◊∞÷√A ’ºØNO∆¯Ã£¨’˝»∑µƒ≤Ÿ◊˜ «__________(ÃÓ–Ú∫≈)°£
a£Æ¥”¢Ÿø⁄Ω¯∆¯£¨”√≈≈ÀÆ∑®ºØ∆¯
b£Æ¥”¢Ÿø⁄Ω¯∆¯£¨”√≈≈∆¯∑®ºØ∆¯
c£Æ¥”¢⁄ø⁄Ω¯∆¯£¨”√≈≈ÀÆ∑®ºØ∆¯
d£Æ¥”¢⁄ø⁄Ω¯∆¯£¨”√≈≈∆¯∑®ºØ∆¯
[ µ—È∂˛]Œ™¡ÀÃΩæø∂∆–ø±°Ã˙∞Â…œ–øµƒ÷ ¡ø∑÷ ˝w(Zn)∫Õ∂∆≤„∫Ò∂»£¨≤ȗص√÷™–ø“◊»Ð”⁄«øºÓ£∫Zn+2NaOH===Na2ZnO2+H2°¸°£æð¥À£¨Ωÿ»°√ʪ˝Œ™SµƒÀ´√Ê∂∆–ø±°Ã˙∞ ‘—˘£¨ºÙÀÈ°¢≥∆µ√÷ ¡øŒ™m1 g°£”√πÃÃÂ…’ºÓ∫ÕÀÆ◊ˆ ‘º¡£¨ƒ‚≥ˆœ¬¡– µ—È∑Ω∞∏≤¢Ω¯––œýπÿ µ—È°£
∑Ω∞∏º◊£∫Õ®π˝≤‚¡ø ‘—˘”κÓ∑¥”¶…˙≥…µƒ«‚∆¯Ãª˝¿¥ µ—ÈÃΩæøƒø±Í°£
(2)—°”√B∫Õ__________(ÃÓ“«∆˜±Í∫≈)¡Ω∏ˆ◊∞÷√Ω¯–– µ—È°£
(3)≤‚µ√≥‰∑÷∑¥”¶∫Û…˙≥…«‚∆¯µƒÃª˝Œ™V L(±Í◊º◊¥øˆ)£¨w(Zn)£Ω__________°£
(4)º∆À„∂∆≤„∫Ò∂»£¨ªπ–˺ÏÀ˜µƒ“ª∏ˆŒÔ¿Ì¡ø «________°£
(5)»Ù◊∞÷√B÷–µƒ∫„—π∑÷“∫¬©∂∑∏ƒŒ™∆’Õ®∑÷“∫¬©∂∑£¨≤‚¡øΩ·π˚Ω´__________(ÃÓ°∞∆´¥Û°±°∞∆´–°°±ªÚ°∞ŒÞ”∞œÏ°±)°£
∑Ω∞∏““£∫Õ®π˝≥∆¡ø ‘—˘”κÓ∑¥”¶«∞∫Ûµƒ÷ ¡ø µœ÷ÃΩæøƒø±Í°£—°”√“«∆˜C◊ˆ µ—È£¨ ‘—˘æ≠≥‰∑÷∑¥”¶£¨¬À≥ˆ≤ª»ÐŒÔ°¢œ¥µ”°¢∫Ê∏…°¢≥∆µ√∆‰÷ ¡øŒ™m2 g°£
(6)w(Zn)£Ω__________°£
∑Ω∞∏±˚£∫Õ®π˝≥∆¡ø ‘—˘”κÓ∑¥”¶«∞∫Û“«∆˜°¢ ‘—˘∫Õ ‘º¡µƒ◊Ð÷ ¡ø(∆‰≤Ó÷µº¥Œ™H2µƒ÷ ¡ø) µœ÷ÃΩæøƒø±Í°£ µ—ÈÕ¨—˘ π”√“«∆˜C°£
(7)¥” µ—ÈŒÛ≤ÓΩ«∂»∑÷Œˆ£¨∑Ω∞∏±˚__________∑Ω∞∏““(ÃÓ°∞”≈”⁄°±°∞¡””⁄°±ªÚ°∞µ»Õ¨”⁄°±)°£
Ω‚Œˆ£∫±æÂøº≤È∂®¡øªØ—ß µ—È°£(1)≥£Œ¬œ¬NO”Ηı∆¯∑¢…˙∑¥”¶£¨π ≤ªƒÐ”√≈≈ø’∆¯∑® ’ºØ°£≈≈ÀÆ∑® ’ºØ∆¯Ã”¶◊¢“‚µºπеƒ°∞∂ÃΩ¯≥§≥ˆ°±°£(2)BŒ™÷∆»°∆¯Ãµƒ∑¥”¶◊∞÷√£¨∂¯DŒ™¡ø∆¯◊∞÷√°£(3)∏˘æðªØ—ß∑Ω≥Ã Ω£¨ZnµƒŒÔ÷ µƒ¡øµ»”⁄«‚∆¯µƒŒÔ÷ µƒ¡ø£¨w(Zn)£Ω°¡65 g/mol°¬m1£Ω°£(4)“—÷™√ʪ˝£¨º∆À„∆‰∫Ò∂»–Ë“™Ãª˝º¥ø…£¨Zn÷ ¡øø…“‘º∆À„£¨“Ú¥À–Ë“™ºÏÀ˜µƒŒÔ¿Ì¡øŒ™√Ð∂»°£(5)∫„—π∑÷“∫¬©∂∑∏ƒŒ™∆’Õ®∑÷“∫¬©∂∑£¨‘Ú∆¯ÃÂ∑¢…˙◊∞÷√÷–µƒ∆¯—π∏þ”⁄¥Û∆¯—𣨑ÚD◊∞÷√∂¡ ˝∆´¥Û°£(6)¡Ω¥Œ÷ ¡ø≤Óº¥Œ™∑¥”¶µƒZnµƒ÷ ¡ø°£(7)∑Ω∞∏±˚÷–”…”⁄∑¥”¶∑≈»»£¨µº÷¬»Ð“∫÷–ÀÆ’Ù∑¢£¨¥”∂¯÷¬ π≤‚∂®Ω·π˚ŒÛ≤ÓΩœ¥Û°£
¥∞∏£∫(1)c°°(2)D
(3)(ªÚµ»∆‰À˚∫œ¿Ì¥∞∏)
(4)Ω Ù–øµƒ√Ð∂»
(5)∆´¥Û
(6)(ªÚ∆‰À˚∫œ¿Ì¥∞∏)
(7)¡””⁄
21£Æ“—÷™ƒ≥∞◊…´∑€ƒ©÷ª”–K2SO4°¢NH4HCO3°¢KCl°¢NH4Cl°¢CuSO4ŒÂ÷÷ŒÔ÷ ÷–µƒ¡Ω÷÷£¨Œ™ºÏ—È∏√∞◊…´∑€ƒ©µƒ≥…∑÷£¨«ÎÕÍ≥…œ¬¡– µ—È£∫
µ—È“ª£∫»° ¡ø∏√∞◊…´∑€ƒ©”⁄…’±≠÷–£¨º”’Ù¡ÛÀÆ»ÐΩ‚£¨µ√µΩŒÞ…´Õ∏√˜»Ð“∫A°£Ω´»Ð“∫A∑÷≥…¡Ω∑ð£¨∑÷±◊∞”⁄¡Ω÷ß ‘πÐ÷–£¨œÚ∆‰÷–“ª÷ß ‘πпԵŒº”œ°œıÀ·£¨”–ŒÞ…´∆¯≈ð≤˙…˙°£
”…¥À≈–∂œ£¨∏√∞◊…´∑€ƒ©÷–øœ∂®∫¨”–__________£¨øœ∂®≤ª∫¨”–__________°£
µ—È∂˛£∫
|
¥˝ºÏ—ÈŒÔ÷ |
µ—È≤Ÿ◊˜ |
‘§∆⁄œ÷œÛ∫ÕΩ·¬€ |
|
K2SO4 |
œÚ ¢”–»Ð“∫Aµƒ¡Ì“ª÷ß ‘πÐ÷–µŒº”__________»Ð“∫ |
°° |
µ—È»˝£∫
|
µ—È«∞÷ |
µ—È≤Ÿ◊˜ |
‘§∆⁄œ÷œÛ∫ÕΩ·¬€ |
|
»Ù∞◊…´ ∑€ƒ©÷–≤ª ∫¨K2SO4 |
»°…Ÿ¡ø‘≠πÃêÏ∫œŒÔ”⁄ ‘πÐ÷–£¨”√æ∆æ´µ∆≥‰∑÷º”»» |
»Áπ˚ ‘πе◊≤ø”–πÃÃÂ≤–¡Ù£¨‘ÚªÏ∫œŒÔ÷–∫¨”–________£ª»Áπ˚ ‘πе◊≤øŒÞπÃÃÂ≤–¡Ù£¨‘ÚªÏ∫œŒÔ÷–∫¨”–__________ |
¥∞∏£∫ µ—È“ª£∫NH4HCO3°°CuSO4
µ—È∂˛£∫BaCl2°°»Ù≥ˆœ÷∞◊…´≥¡µÌ£¨‘Ú∫¨”–K2SO4
µ—È»˝£∫NH4HCO3∫ÕKCl°°NH4HCO3∫ÕNH4Cl
20£Æ∏þ√ÃÀ·ºÿÀ◊≥∆PP∑€£¨Œ™«ø—ıªØº¡£¨”ˆµΩ”–ª˙ŒÔæÕ∑≈≥ˆªÓ–‘—ı°£’‚÷÷—ı”–…±√œ∏æ˙µƒ◊˜”√£¨«“…±æ˙ƒÐ¡¶º´«ø°£ƒ≥—ß…˙”˚‘⁄ µ—È “≈‰÷∆1 L 0.06 mol/L KMnO4œ°»Ð“∫£¨”√¿¥«Âœ¥…Àø⁄°£
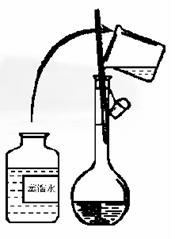
(1) µ—Èπ˝≥Ã÷––Ë”√Õ–≈ÃÃÏ∆Ω≥∆»°KMnO4æßõƒ÷ ¡øŒ™__________g°£
(2)∆‰≤Ÿ◊˜≤Ω÷Ë»Áœ¬ÕºÀ˘ 棨‘Ú”“ÕºÀ˘ æ≤Ÿ◊˜”¶‘⁄œ¬Õº÷–__________(ÃÓ—°œÓ◊÷ƒ∏)÷ƺ‰°£
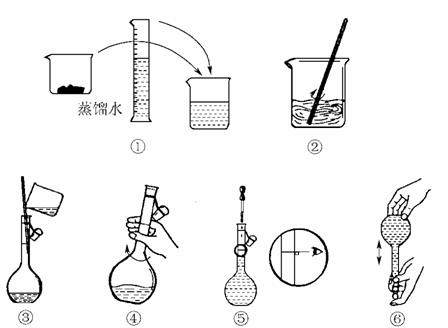
A£Æ¢⁄”΢€°°B£Æ¢Ÿ”΢⁄°°C£Æ¢Ð”΢ð
(3)»Ù∏√Õ¨—ß‘⁄≈‰÷∆»Ð“∫ ±£¨Ω¯––¡À»Áœ¬≤Ÿ◊˜£¨∆‰÷– πÀ˘≈‰»Ð“∫≈®∂»∆´µÕµƒ≤Ÿ◊˜”–__________(ÃÓ—°œÓ◊÷ƒ∏)°£
A£Æ≥∆¡øKMnO4æßà±£¨÷∏’Î∆´œÚ”“±þ
B£ÆΩ´KMnO4æßÃÂ∑≈‘⁄…’±≠÷–»ÐΩ‚£¨¿‰»¥∫Û£¨◊™“∆÷¡∫¨”–…Ÿ¡ø’Ù¡ÛÀƵƒ»ð¡ø∆ø÷–
C£Æ∂®»ð ±£¨—ˆ ”øÃ∂»œþ
D£Æ’Òµ¥“°‘»∫Û£¨∑¢œ÷»Ð“∫“∫√ʵՔ⁄øÃ∂»œþ£¨‘ŸµŒº”…Ÿ¡ø’Ù¡ÛÀÆ÷¡øÃ∂»œþ¥¶
Ω‚Œˆ£∫m(KMnO4)£Ω1°¡0.06°¡158£Ω9.48(g)°÷9.5 g°£
¥∞∏£∫(1)9.5°°(2)C°°(3)ACD
19£Æƒ≥Õ¨—ߌ™¡À≤‚∂®»˝æ€«Ë∞∑µƒ∑÷◊” Ω£¨…˺∆¡À»Áœ¬ µ—È£∫
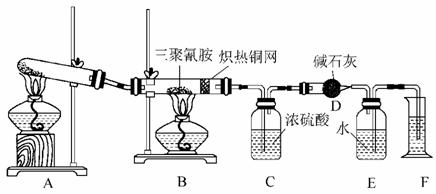
≤È‘ƒ◊ ¡œ£¨»˝æ€«Ë∞∑µƒœý∂‘∑÷◊”÷ ¡øŒ™126£¨»˝æ€«Ë∞∑‘⁄≥£Œ¬œ¬Œ™æß㨑⁄º”»»Ãıº˛œ¬ƒÐ”Ηı∆¯∑¢…˙∑¥”¶…˙≥…∂˛—ıªØú°¢µ™∆¯∫ÕÀÆ°£»°12.6 g»˝æ€«Ë∞∑æßÃÂ∞¥Õº æ µ—È∑¥”¶(ºŸ…Ë»˝æ€«Ë∞∑ÕÍ»´◊™ªØ≥…≤˙ŒÔ)°£
(1)–¥≥ˆA◊∞÷√÷–∑¢…˙∑¥”¶µƒªØ—ß∑Ω≥à Ω________________________________________°£
(2)C◊∞÷√ƒÐ≤ªƒÐ”ÎD◊∞÷√ª•ªª£ø__________(ÃÓ°∞ƒÐ°±ªÚ°∞≤ªƒÐ°±)°£¿Ì”… «____________________________°£
(3)µ±B◊∞÷√÷–∑¥”¶ÕÍ»´∑¢…˙∫Û£¨∂¡»°F÷–ÀƵƒÃª˝µƒ µ—È≤Ÿ◊˜À≥–ÚŒ™__________(ÃÓ–Ú∫≈)°£
¢Ÿ∂¡ ˝°°¢⁄¿‰»¥÷¡ “Œ¬°°¢€µ˜∆ΩE°¢F◊∞÷√÷–µƒ“∫√Ê
(4)≤‚∂® ˝æð»Áœ¬£∫
|
◊∞÷√ |
C |
D |
|
µ—È«∞ |
101.0 g |
56.0 g |
|
µ—È∫Û |
106.4 g |
69.2 g |
æ≠≤‚∂®£¨E÷– ’ºØµƒ∆¯ÃÂ’€∫œ≥…±Í◊º◊¥øˆœ¬µƒÃª˝Œ™6.72 L°£
¢Ÿ¿˚”√…œ ˆ µ—È ˝æ𣨺∆À„»˝æ€«Ë∞∑µƒ µ—È ΩŒ™__________°£
¢⁄»˝æ€«Ë∞∑∑÷◊” ΩŒ™__________°£
¢€»ÙB◊∞÷√÷–√ª”–Õ≠Õ¯£¨∂‘≤‚∂®Ω·π˚µƒ”∞œÏ «__________________________________°£
Ω‚Œˆ£∫(1)∏˘æð µ—È‘≠¿Ì÷™£∫A◊∞÷√”√”⁄÷∆»°—ı∆¯£¨«“≤…”√º”»»πÃõƒ∑Ω∑®÷∆—ı∆¯£ª(2)ºÓ ت“º»ƒÐŒ¸ ’∂˛—ıªØú”÷ƒÐŒ¸ ’ÀÆ£¨∂¯≈®¡ÚÀ·÷ªŒ¸ ’ÀÆ£¨≤ªƒÐŒ¸ ’∂˛—ıªØú£ª(4)C◊∞÷√‘ˆº”µƒ÷ ¡øæÕ «ÀƵƒ÷ ¡ø£¨D◊∞÷√‘ˆº”µƒ÷ ¡øæÕ «∂˛—ıªØúµƒ÷ ¡ø£¨n(CO2)£Ω(69.2£≠56.0) g/44 g/mol£Ω0.3 mol£¨n(H2O)£Ω(106.4£≠101.0) g/18 g/mol£Ω0.3 mol£¨n(N2)£Ω6.72 L/22.4 L/mol£Ω0.3 mol°£‘Ú∑¥”¶ŒÔ÷–C°¢H°¢N‘™Àÿµƒ◊Ð÷ ¡ø£Ω0.3 mol°¡12 g/mol+0.6 mol°¡1 g/mol+0.6 mol°¡14 g/mol£Ω12.6 g£¨Àµ√˜—˘∆∑≤ª∫¨—ı‘™Àÿ°£À˘“‘»˝æ€«Ë∞∑∑÷◊”÷–£¨n(C)°√n(H)°√n(N)£Ω0.3 mol°√0.6 mol°√0.6 mol£Ω1°√2°√2£¨…Ë»˝æ€«Ë∞∑µƒ∑÷◊” ΩŒ™(CH2N2)n£¨‘Ú(12+2+28)n£Ω126£¨n£Ω3£¨π ∆‰∑÷◊” ΩŒ™C3H6N6°£»ÙB◊∞÷√÷–√ª”–Õ≠Õ¯£¨ø…ƒÐ”–√ª”–∑¥”¶µƒ—ı∆¯Ω¯»ÎE∆ø÷–£¨µº÷¬≤‚∂®µƒµ™∆¯Ãª˝∆´¥Û£¨º¥≤‚∂®µ√µΩµƒ»˝æ€«Ë∞∑∑÷◊” Ω÷–µ™‘≠◊” ˝∆´¥Û£¨∂¯Ãº°¢«‚‘≠◊” ˝∆´–°°£
¥∞∏£∫(1)2KMnO4°˜K2MnO4+MnO2+O2°¸ªÚ2KClO3MnO2°˜2KCl+3O2°¸°°(2)≤ªƒÐ°° µ—È÷–≈®¡ÚÀ·Œ¸ ’ÀÆ£¨ºÓ ت“Œ¸ ’∂˛—ıªØú£¨»Ùª•ªª£¨ºÓ ت“ƒÐÕ¨ ±Œ¸ ’∂˛—ıªØú∫ÕÀÆ£¨µº÷¬ µ—È ß∞а°(3)¢⁄¢€¢Ÿ°°(4)CH2N2°°C3H6N6°° π≤‚∂®À˘µ√µƒ»˝æ€«Ë∞∑∑÷◊” Ω÷–µ™‘≠◊” ˝∆´¥Û£¨Ãº°¢«‚‘≠◊” ˝∆´–°
18£Æ µ—È “”√÷ ¡ø∑÷ ˝Œ™98%°¢√Ð∂»Œ™1.84 g/cm3µƒ≈®¡ÚÀ·≈‰÷∆100 g 10%µƒH2SO4»Ð“∫°£≈‰÷∆π˝≥Ã÷––Ë“™”√µΩµƒ“«∆˜”–(°°)
¢ŸÕ–≈ÃÃÏ∆Ω°°¢⁄10 mL¡øÕ≤°°¢€100 mL¡øÕ≤°°¢Ð…’±≠°°¢ð≤£¡ß∞Ù°°¢Þ100 mL»ð¡ø∆ø°°¢þΩ∫Õ∑µŒπÐ
A£Æ¢⁄¢€¢Ð¢ð¢þ°°°°°°B£Æ¢⁄¢Ð¢ð¢Þ¢þ
C£Æ¢Ÿ¢Ð¢ð¢Þ¢þ°° D£Æ¢⁄¢€¢Ð¢ð¢Þ¢þ
Ω‚Œˆ£∫Ω´“ª∂®Ãª˝µƒ≈®H2SO4œ° Õ≈‰÷∆“ª∂®÷ ¡ø∑÷ ˝µƒ»Ð“∫£¨≤ª–Ë“™»ð¡ø∆ø°£
¥∞∏£∫A
µ⁄¢ÚæÌ(∑«—°‘Ò£¨π≤46∑÷)
17£Æœ¬¡–ŒÔ÷ ∑÷¿Îπ˝≥Ã÷–…ʺ∞π≤º€º¸∂œ¡—µƒ «(°°)
A£Æ”√…¯Œˆ∑®≥˝»•µÌ∑€Ω∫ÃÂ÷–µƒ…Ÿ¡øNaCl
B£Æ”√±•∫Õ ≥—ŒÀÆœ¥»•Cl2÷–µƒ…Ÿ¡øHCl
C£Æ”√CCl4ðÕ»°µ‚ÀÆ÷–µƒµ‚
D£Æ”√…˝ª™∑®≥˝»•NaCl÷–ªÏ”–µƒ…Ÿ¡øµ‚
Ω‚Œˆ£∫AœÓ¿˚”√NaClƒÐÕ∏π˝∞ÎÕ∏ƒ§∂¯Ω∫ÃÂ≤ªƒÐÕ∏π˝µƒ–‘÷ £ªBœÓHCl‘⁄»ÐΩ‚µƒπ˝≥Ã÷–∂œ¡—¡Àπ≤º€º¸£ªCœÓΩˆ «µ‚‘⁄CCl4÷–»ÐΩ‚£ªDœÓµ‚…˝ª™µƒπ˝≥Ã÷–∆∆ªµµƒ «∑÷◊”º‰◊˜”√¡¶°£
¥∞∏£∫B
16£Æœ¬¡–Àµ∑®’˝»∑µƒ «(°°)
A£Æ±Ω∑”’¥‘⁄ ÷…œ£¨”¶¡¢º¥”√NaOH»Ð“∫«Âœ¥
B£Æ∏¯ ‘πÐ÷–“∫ú”»» ±£¨“∫ÃÂ≤ª≥¨π˝ ‘πÐ»ðª˝µƒ1/3
C£Æ”√…˝ª™∑®∑÷¿Îµ‚∫Õ¬»ªØÔßµƒªÏ∫œŒÔ
D£Æ ‘πб⁄…œµƒ“¯æµø…”√œ°¡ÚÀ·œ¥µ”
Ω‚Œˆ£∫±Ω∑”’¥‘⁄ ÷…œ£¨”¶¡¢º¥”√æ∆æ´«Âœ¥£¨A—°œÓ¥ÌŒÛ£ªº”»»µ‚…˝ª™£¨¬»ªØÔß∑÷Ω‚£¨”ˆ¿‰µ‚ƒ˝ª™£¨NH3”ÎHClªØ∫œ≥…NH4Cl£¨π ¡Ω’þ≤ªƒÐ∑÷¿Î£¨C—°œÓ¥ÌŒÛ£ª ‘πб⁄…œµƒ“¯ø…”√œ°HNO3œ¥µ”£¨D—°œÓ¥ÌŒÛ°£
¥∞∏£∫B
15£ÆΩ´Mg°¢Al°¢Zn◊È≥…µƒªÏ∫œŒÔ”Î◊„¡ø—ŒÀ·◊˜”√£¨∑≈≥ˆH2µƒÃª˝Œ™2.8 L(±Í◊º◊¥øˆœ¬)£¨‘Ú»˝÷÷Ω ÙµƒŒÔ÷ µƒ¡ø÷Æ∫Õø…ƒÐŒ™(°°)
A£Æ0.250 mol°° B£Æ0.125 mol
C£Æ0.100 mol°° D£Æ0.080 mol
Ω‚Œˆ£∫«‚∆¯ŒÔ÷ µƒ¡øŒ™ mol£Ω0.125 mol°£»Ù»´≤øŒ™MgªÚZn£¨Ω ÙµƒŒÔ÷ µƒ¡øŒ™0.125 mol£ª»Ù»´≤øŒ™Al£¨Ω ÙµƒŒÔ÷ µƒ¡øŒ™0.083 mol£¨π Ω ÙŒÔ÷ µƒ¡ø÷Æ∫Õ‘⁄0.083µΩ0.125 mol÷ƺ‰°£
¥∞∏£∫C
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com