
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
10ЃЎ(2009ЁЄжиЧь)ИїПЩФцЗДгІДяЕНЦНКтКѓЃЌИФБфЗДгІЬѕМўЃЌЦфБфЛЏЧїЪЦе§ШЗЕФЪЧЁЁЁЁЁЁ (ЁЁ)
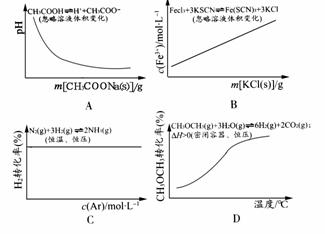
НтЮіЃКAЯюЃКМгШыCH3COONa(s)ЪЙШмвКжаc(CH3COOЃ)діДѓЃЌвжжЦЕчРыЃЌpHдіДѓЃЛBЯюЃКдЦНКтЪЕжЪЮЊFe3++3SCNЃFe(SCN)3МгШыKCl(s)ЮогАЯьЃЛCЯюЃККубЙГфШыArЛсЪЙШнЦїЬхЛ§діДѓ(ЯрЕБгкМѕбЙ)ЃЛDЯюЃКЩ§ИпЮТЖШЃЌЦНКте§ЯђвЦЖЏЁЃ
Д№АИЃКD
9ЃЎЛЏКЯЮяHInдкЫЎШмвКжаДцдквдЯТЕчРыЦНКтЃЌПЩгУзїЫсМюжИЪОМСЃКHIn(aq)(КьЩЋ)H+(aq)+InЃ(aq)(ЛЦЩЋ)ЃЌХЈЖШЮЊ0.02 molЁЄLЃ1ЕФЯТСаИїШмвКЃКЂйбЮЫсЁЁЂкЪЏЛвЫЎЁЁЂлNaClШмвКЁЁЂмNaHSO4ШмвКЁЁЂнNaHCO3ШмвКЁЁЂоАБЫЎЁЃЦфжаФмЪЙжИЪОМСЯдКьЩЋЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ)
AЃЎЂйЂмЂнЁЁ ЁЁЁЁЁЁЁЁ BЃЎЂкЂнЂоЁЁ ЁЁЁЁЁЁЁЁ CЃЎЂйЂмЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎЂкЂлЂо
Д№АИЃКC
8ЃЎНЋpHЯрЭЌЃЌШмвКЬхЛ§вВЯрЭЌЕФСНжжЫсШмвК(МзЃКбЮЫсЃЛввЃКДзЫс)ЗжБ№гыаПЗДгІЃЌШєзюКѓгавЛШмвКжагааПЪЃгрЃЌЧвЗХГіЕФЦјЬхвЛбљЖрЃЌЖдДЫгаШчЯТХаЖЯЃЌЦфжае§ШЗЕФЪЧ(ЁЁ)
(1)ЫљашЪБМфЃКвв<МзЁЁ(2)ПЊЪМЪБЗДгІЫйТЪЃКМз>ввЁЁ(3)ВЮМгЗДгІЕФаПЕФжЪСПЃКМзЃНввЁЁ(4)ећИіЗДгІНзЖЮЕФЦНОљЫйТЪЃКвв>МзЁЁ(5)ЪЂбЮЫсЕФШнЦїжагааПЪЃгрЁЁ(6)ЪЂДзЫсЕФШнЦїжагааПЪЃгр
AЃЎ(1)(2)(3)(5)ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎ(1)(3)(5)
CЃЎ(2)(3)(6)ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎ(1)(3)(4)(5)
НтЮіЃКгЩгкМзЮЊбЮЫсЃЌввЮЊДзЫсЃЌвђДЫСНШмвКH+ЮяжЪЕФСПХЈЖШЯрЭЌЪБЃЌДзЫсЕФЮяжЪЕФСПХЈЖШБШбЮЫсДѓЕУЖрЁЃгжвђСНЗнШмвКЕШЬхЛ§ЃЌЫљвдДзЫсЕФЮяжЪЕФСПБШбЮЫсДѓЕУЖрЁЃгЩгкПЊЪМЗДгІЪБЕФH+ЮяжЪЕФСПХЈЖШЯрЭЌЃЌвђДЫПЊЪМЗДгІЕФЫйТЪЯрЭЌЁЃ
Д№АИЃКD
7ЃЎ(2009ЁЄЩНЖЋЪЁзЭВЉЪаФЃФт)ЗжБ№дкpHЃН1ЕФЫсКЭpHЃН14ЕФNaOHШмвКжаМгШызуСПЕФТСЃЌЗХГіH2ЕФСПЧАепЖрЃЌЦфдвђПЩФмЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ)
ЂйСНШмвКЕФЬхЛ§ЯрЭЌЃЌЫсЪЧЖрдЊЧПЫсЁЁЂкСНШмвКЕФЬхЛ§ЯрЭЌЃЌЫсЪЧвЛдЊШѕЫсЁЁЂлЫсШмвКЕФЬхЛ§ДѓгкNaOHШмвКЕФЬхЛ§ЁЁЂмЫсЪЧЧПЫсЃЌХЈЖШБШNaOHШмвКЕФДѓ
AЃЎЂйЂкЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎЂкЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎЂкЂлЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎЂм
НтЮіЃКВњЩњH2ЕФСПЯрЕШЪБЃЌn(H+)ЃНn(OHЃ)ЃЌВњЩњH2ЖрЃЌдђвЛЖЈЪЧn(H+)>n(OHЃ)ЃЌЖјpHЃН1ЕФЫсжаc(H+)гыpHЃН14ЕФNaOHШмвКжаc(OHЃ)ЯрБШЧАепаЁЃЌЫљвдгаСНжжЧщПіПЩВњЩњЬтЩшНсЙћЃКвЛЪЧЕШЬхЛ§ЪБЃЌЫсЪЧвЛдЊШѕЫсЃЌЖўЪЧЫсЕФЬхЛ§ДѓЁЃД№АИЮЊCЯюЁЃ
Д№АИЃКC
6ЃЎдк25ЁцЪБЃЌ0.1 molЁЄLЃ1ЕФHNO2ЁЂHCOOHЁЂHCNЁЂH2CO3ЕФШмвКЃЌЫќУЧЕФЕчРыЦНКтГЃЪ§ЗжБ№ЮЊ4.6ЁС10Ѓ4mol2ЁЄLЃ2ЁЂ1.8ЁС10Ѓ4mol2ЁЄLЃ2ЁЂ4.9ЁС10Ѓ10mol2ЁЄLЃ2ЁЂK1ЃН4.3ЁС10Ѓ7mol2ЁЄLЃ2КЭK2ЃН5.6ЁС10Ѓ11mol2ЁЄLЃ2ЃЌЦфжаЧтРызгХЈЖШзюаЁЕФЪЧЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ)
AЃЎHNO2ЁЁ ЁЁЁЁЁЁЁЁЁЁ BЃЎHCOOHЁЁ ЁЁЁЁЁЁ CЃЎHCNЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎH2CO3
НтЮіЃКШѕЫсЕФХЈЖШЯрЭЌЪБЃЌKжЕдНаЁ(ЖрдЊШѕЫсПДK1)ЃЌЫсаддНШѕЃЌЧтРызгХЈЖШдНаЁЁЃ
Д№АИЃКC
5ЃЎЧтЗњЫсЪЧШѕЫсЃЌЕчРыЗНГЬЪНЮЊHF H++FЃЃЌДяЕНЕчРыЦНКтЕФБъжОЪЧЁЁ (ЁЁ)
H++FЃЃЌДяЕНЕчРыЦНКтЕФБъжОЪЧЁЁ (ЁЁ)
AЃЎc(H+)ЃНc(FЃ)
BЃЎv(ЕчРы)ЃНv(НсКЯГЩЗжзг)
CЃЎШмвКЯдЫсад
DЃЎЕЅЮЛЪБМфФкЃЌЕчРыЕФHFЗжзгЪ§гыЩњГЩЕФFЃЪ§ЯрЕШ
Д№АИЃКB
4ЃЎЯТСаа№ЪіжаЃЌФмжЄУїФГЮяжЪЪЧШѕЕчНтжЪЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ)
AЃЎШлЛЏЪБВЛФмЕМЕч
BЃЎВЛЪЧРызгЛЏКЯЮяЪЧЙВМлЛЏКЯЮя
CЃЎЫЎШмвКЕФЕМЕчФмСІКмВю
DЃЎШмвКжаДцдкЕчРыЦНКтЃЌЕчРыГіЕФРызгКЭЮДЕчРыЕФЗжзгЙВДц
Д№АИЃКD
3ЃЎ(2009ЁЄНЫеЫежнжабЇИпШ§дТПМ)ЯТСаЮяжЪАДДПОЛЮяЁЂЛьКЯЮяЁЂЧПЕчНтжЪЁЂШѕЕчНтжЪЁЂЗЧЕчНтжЪЕФзщКЯжаЃЌе§ШЗЕФЪЧЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ)
|
ЁЁ |
ДПОЛЮя |
ЛьКЯЮя |
ЧПЕчНтжЪ |
ШѕЕчНтжЪ |
ЗЧЕчНтжЪ |
|
A |
бЮЫс |
ЫЎУКЦј |
СђЫс |
ДзЫс |
HD |
|
B |
БљДзЫс |
ИЃЖћТэСж |
ПСадМи |
HI |
ввДМ |
|
C |
Л№Мю |
есЬЧШмвК |
ТШЛЏФЦ |
АБЫЎ |
Ш§бѕЛЏСђ |
|
D |
ЕЈЗЏ |
ЪЏЛвЫЎ |
СђЫсБЕ |
HNO2 |
NH3 |
Д№АИЃКD
2ЃЎЯТСаЕчРыЗНГЬЪНЪщаДе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ)
AЃЎNH3ЁЄH2O===NH+OHЃ
BЃЎNaHCO3===Na++HCOЁЁHCOH++CO
CЃЎH2CO3 2H++CO
2H++CO
DЃЎCa(OH)2 Ca2++2OHЃ
Ca2++2OHЃ
Д№АИЃКB
1ЃЎ(2009ЁЄЩЯКЃЫЩНЖўжаИпШ§Цкжа)ЯТСаЕчНтжЪдкЫЎШмвКжаКЭШлШкзДЬЌЯТОљФмЕМЕчЕФЪЧ
(ЁЁ)
AЃЎСђЫсЁЁЁЁЁЁЁЁЁЁ BЃЎЬМЫсИЦЁЁЁЁЁЁ CЃЎЧтбѕЛЏФЦЁЁ DЃЎбѕЛЏУО
Д№АИЃКC
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com